|
在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g) | |
A. |
加催化剂同时升高温度 |
B. |
加催化剂同时增大压强 |
C. |
升高温度同时充入N2 |
D. |
降低温度同时增大压强 |
|
已知反应A2(g)+2B2(g) | |
A. |
升高温度,正向反应速率增加,逆向反映速率减小 |
B. |
升高温度有利于反应速率增加,从而缩短达到平衡的时间 |
C. |
达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 |
D. |
达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
|
一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g) | |
A. |
2 mol C |
B. |
2 mol A、1 mol B和1 mol He(不参加反应) |
C. |
1 mol B和1 mol C |
D. |
2 mol A、3 mol B和3 mol C |
|
如图是温度和压强对X+Y
| |
A. |
上述可逆反应的正反应为放热反应 |
B. |
X、Y、Z均为气态 |
C. |
X和Y中只有一种为气态,Z为气态 |
D. |
上述反应的逆反应的ΔH>0 |
|
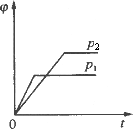
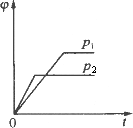
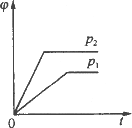
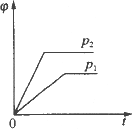
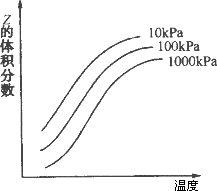
某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):根据以上规律判断,下列结论正确的是
| |
A. |
反应Ⅰ:ΔH>0,P2>P1 |
B. |
反应Ⅱ:ΔH<0,T1>T2 |
C. |
反应Ⅲ:ΔH>0,T2>T1;或ΔH<0,T2<T1 |
D. |
反应Ⅳ:ΔH<0,T2>T1 |
|
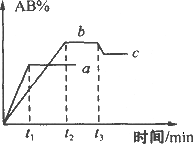
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)
| |
A. |
点a的正反应速率比点b的大 |
B. |
点c处反应达到平衡 |
C. |
点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
D. |
其他条件不变,773 K下反应至t1时刻,n(H2)比上图中d点的值大 |
|
在一定条件下,反应A2+B2
| |
A. |
Q>0 |
B. |
Q<0 |
C. |
Q=0 |
D. |
无法判断 |
|
某温度下在密闭容器中发生如下反应: 2M(g)+N(g) | |
A. |
20% |
B. |
40% |
C. |
60% |
D. |
80% |
|
在恒温时,一固定容积的容器内发生如下反应:2NO2(g) | |
A. |
不变 |
B. |
增大 |
C. |
减小 |
D. |
无法判断 |