|
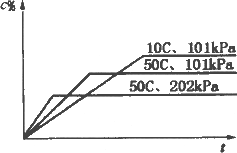
在密闭容器中进行下列可逆反应:A(g)+B(g)
| |
A. |
正反应为放热,D为气态 |
B. |
正反应吸热,D为气态 |
C. |
正反应放热,D为液态 |
D. |
正反应吸热,D为固态 |
|
将装有1 mol HI的容器密封并加热,部分HI分解成H2和I2(g)并达到化学平衡,此时I2(g)的体积分数为x%.若在该容器中加入2 mol HI后密封,加热到相同温度使之达到平衡时,设此时I2(g)的体积分数为y%,则x与y的关系为 | |
A. |
x>y |
B. |
x<y |
C. |
x=y |
D. |
x≥y |
|
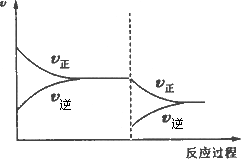
如图表示在某容器中,充入N2和H2,在一定条件下N2+3H2
| |
A. |
可逆反应达到平衡后,又充入N2并建立新的平衡 |
B. |
可逆反应达到平衡后,再减小压强并建立新的平衡 |
C. |
可逆反应达到平衡后,再升高温度并建立新的平衡 |
D. |
可逆反应达到平衡后,减小氨气的浓度并建立新的平衡 |
|
一定温度下,某密闭容器里发生如下可逆反应:CO(g)+H2O(g) | |
A. |
升高温度 |
B. |
增大压强 |
C. |
再通入n mol CO和n mol H2(g) |
D. |
再通入2n mol CO2和2n mol H2 |
|
在一密闭容器中,反应aA(g) | |
A. |
平衡向正反应方向移动了 |
B. |
物质A的转化率减少了 |
C. |
物质B的质量分数增加了 |
D. |
a>b |
|
反应NH4HS(s) | |
A. |
某他条件不变时,通入SO2气体 |
B. |
移走一部分NH4HS固体 |
C. |
容器体积不变,充入N2 |
D. |
压强不变时,充入N2 |
|
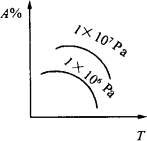
A%为气态反应物在平衡体系中的百分含量,符合曲线的反应是
| |
A. |
N2(g)+3H2(g) |
B. |
C(s)+CO2(g) |
C. |
N2(g)+O2(g) |
D. |
CaCO3(s) |
|
在一定温度下,密闭容器中加入H2和I2(g)各0.5 mol发生反应:H2(g)+I2(g) | |
A. |
仍为0.8 mol |
B. |
1 mol |
C. |
大于0.8 mol,小于1 mol |
D. |
大于1 mol |
|
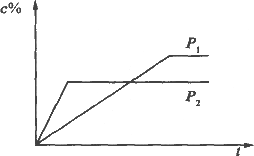
在温度相同,压强分别为P1和P2的条件下,A(g)+2B(g)
| |
A. |
P1>P2,n<3 |
B. |
P1<P2,n>3 |
C. |
P1>P2,n>3 |
D. |
P1<P2,n<3 |
|
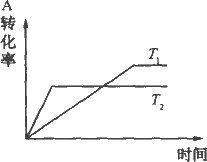
mA(g)+nB(g)
| |
A. |
T1>T2,正反应是吸热反应 |
B. |
T1<T2,正反应是放热反应 |
C. |
T1<T2,正反应是吸热反应 |
D. |
T1>T2,正反应是放热反应 |