|
用铂电极电解CuSO4溶液,在阳极收集到0.4 g O2,中和电解时生成的酸用去250 mL NaOH溶液,则此NaOH溶液物质的量浓度是 | |
A. |
0.05 mol/L |
B. |
0.10 mol/L |
C. |
0.15 mol/L |
D. |
0.20 mol/L |
|
以碳棒做电极,以同等强度的电流同时电解下列体积相同的溶液,最先终止反应的是 | |
A. |
0.1 mol/L H2SO4 |
B. |
0.4 mol/L NaOH |
C. |
0.3 mol/L KNO3 |
D. |
0.5 mol/L HCl |
|
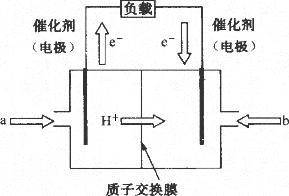
如图是2004年批量生产的笔记本电脑所用甲醇燃料电池的结构示意图.
甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应.该电池总反应式为2CH3OH+3O2 | |
A. |
左电极为电池的负极,a处通入的物质是甲醇 |
B. |
右电极为电池的负极,b处通入的物质是空气 |
C. |
负极反应式为CH3OH+H2O-6e- |
D. |
正极反应式为O2+2H2O+4e- |
|
通以相等的电量,分别电解等浓度的硝酸银硝酸亚汞(亚汞的化合价为+1)溶液,若被还原的硝酸银和硝酸亚汞的物质的量之比n(硝酸银)∶n(硝酸亚汞)=2∶1,则下列表达正确的是 | |
A. |
在两个阴极上得到的银和汞的物质的量之比n(银)∶n(汞)=4∶1 |
B. |
在两个阳极上得到的产物的物质的量不相等 |
C. |
硝酸亚汞的分子式为Hg2(NO3)3 |
D. |
硝酸亚汞的分子式为Hg2(NO3)2 |
|
在铁制品上镀一定厚度的锌层,以下方案设计正确的是 | |
A. |
锌作阳极,镀件作阴极,溶液中含有锌离子 |
B. |
铂作阴极,镀件作阳极,溶液中含有锌离子 |
C. |
铁作阳极,镀件作阴极,溶液中含有亚铁离子 |
D. |
锌作阴极,镀件作阳极,溶液中含有锌离子 |
|
若某电能与化学能的转化装置(电解池或原电池)中发生反应的总反应离子方程式是Cu+2H+ | |
A. |
该装置可能是原电池,也可能是电解池 |
B. |
该装置只能是原电池,且电解质溶液为硝酸 |
C. |
该装置只能是电解池,且金属铜为该电解池的阳极 |
D. |
该装置只能是电解池,电解质溶液不可能是盐酸 |