|
将质量分数为98%、密度为1.84 g·cm-3的浓H2SO4 10 mL,慢慢倒入100 mL水中稀释后所得稀H2SO4的质量分数的计算式正确的是 | |
A. |
|
B. |
|
C. |
|
D. |
|
|
浓硫酸和2 mol·L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如下图.分析a、b曲线变化的原因是
| |
A. |
a升华、b冷凝 |
B. |
a挥发、b吸水 |
C. |
a蒸发、b潮解 |
D. |
a冷凝、b吸水 |
|
下列对浓硫酸的叙述正确的是 | |
A. |
常温下,浓硫酸与铁、铝不反应,所以铁质、铝质容器能盛放浓硫酸 |
B. |
浓硫酸具有吸水性,能使蔗糖碳化 |
C. |
浓硫酸和铜片加热既表现强酸性,又表现出强氧化性 |
D. |
浓硫酸与亚硫酸钠反应制取二氧化硫时,浓硫酸表现出强氧化性 |
|
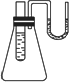
如图所示,小试管内盛有约3 mL饱和硫酸铜溶液,与锥形瓶连通的U形细管内盛有少量水(为便于观察,预先染成红色),沿小试管的内壁小心地慢慢倒入约3 mL浓硫酸,静置片刻.可观察的现象有
| |
A. |
小试管内液体分成两层,上层蓝色,下层无色 |
B. |
U形细管内左边液面下降,右边液面升高 |
C. |
有少量的白色固体析出 |
D. |
以上现象都没有,无明显变化 |