|
H2A为二元弱酸,则下列说法正确的是 | |
| [ ] | |
A. |
在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等 |
B. |
在等物质的量浓度的Na2A、NaHA两溶液中,前者pH大于后者 |
C. |
在NaHA溶液中一定有:c(Na+)>c(HA-)>c(OH-)>c(H+) |
D. |
在Na2A溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+c(A2-) |
|
一些烷烃的燃烧热如下表:
下列表达正确的是 | |
| [ ] | |
A. |
正戊烷的燃烧热小于3 531.3 kJ·mol-1 |
B. |
稳定性:正丁烷<异丁烷 |
C. |
乙烷的燃烧热化学方程式为:2C2H6(g)+7O2(g) |
D. |
相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多 |
|
某有机化合物A的相对分子质量大于100,小于130.经分析得知,其中碳和氢的质量分数之和为46.66%,其余为氧,则该化合物分子中最多含碳氧双键的个数为 | |
| [ ] | |
A. |
1 |
B. |
2 |
C. |
3 |
D. |
4 |
|
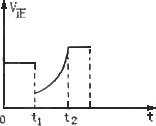
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g)=-2NH3(g) ΔH=-92.4 kJ·mol-1)
下列说法正确的是 | |
| [ ] | |
A. |
2c1>c3 |
B. |
a+b=92.4 |
C. |
2p2<p3 |
D. |
a1+a2>1 |
|
浓度为2 mol·L-1的氢溴酸溶液VL,欲使其浓度变为4 mol·L-1,以下列出的方法中,可行的为 | |
| [ ] | |
A. |
通入标况下的HBr气体44.8 L |
B. |
加入10 mol·L-1氢溴酸0.6 VL,再将溶液稀释至2 VL |
C. |
蒸发掉0.5 L水 |
D. |
将溶液加热蒸发浓缩至0.5 V |
|
如图所示,表示反应2SO2(g)+O2
| |
| [ ] | |
A. |
t1时增加了SO2和O2的浓度,平衡向正反应方向移动; |
B. |
t1降低了温度,平衡向正反应方向移动; |
C. |
t1时减小了压强,平衡向逆反应方向移动; |
D. |
t1时减小了SO2的浓度,增加了SO3的浓度,平衡向逆反应方向移动 |
|
已知N2(g)+3H2(g) | |
| [ ] | |
A. |
1.5,6.5 |
B. |
2,8 |
C. |
5,21 |
D. |
3,13 |
|
某烷烃的各种同分异构体中,主链上有4个碳原子的只有两种结构,则含相同碳原子数且主链上也有4个碳原子的烯烃(只含一个碳碳双键)的同分异构体有(不考虑顺反异构) | |
| [ ] | |
A. |
2种 |
B. |
3种 |
C. |
4种 |
D. |
5种 |
|
将2 mol SO2,1 mol O2充入带活塞的密闭容器中,发生反应2SO2(g)+O2(g) | |
| [ ] | |
A. |
保持温度和容器的压强不变,充入1 mol SO3(g) |
B. |
保持温度和容器的容积不变,充入1 mol SO3(g) |
C. |
保持温度和容器的压强不变,充入1 mol O2(g) |
D. |
保持温度和容器的压强不变,充入1 mol Ar |
|
铁-镍蓄电池放电和充电时发生的反应为: Fe+NiO2+2H2O 关于此蓄电池的下列说法中不正确的是 | |
| [ ] | |
A. |
放电时铁为负极 |
B. |
充电时阴极的电极反应式为:Ni(OH)2-2e- |
C. |
放电时NiO2的反应为:NiO2+2H2O+2e- |
D. |
蓄电池的电极必须浸在碱性电解质溶液中 |

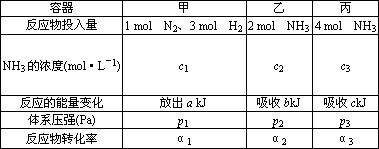
 2SO3(g),ΔH<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是
2SO3(g),ΔH<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是