|
将足量的铝粉分别加入下列100 ml溶液中,充分反应后,放出氢气最多的是 | |
| [ ] | |
A. |
3 mol·L-1 HCl |
B. |
4 mol·L-1 HNO3 |
C. |
8 mol·L-1 NaOH |
D. |
5 mol·L-1 H2SO4 |
|
化学在生产和日常生活中有着重要的应用.下列说法不正确的是 | |
| [ ] | |
A. |
明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
B. |
家庭使用的“84”消毒液主要成分是NaClO |
C. |
MgO的熔点很高,可用于制作耐高温材料 |
D. |
电解MgCl2饱和溶液,可制得金属镁 |
|
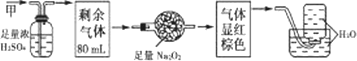
无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100 mL甲气体经过下图所示实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为
| |
| [ ] | |
A. |
NH3、NO2、O2 |
B. |
NH3、NO、CO2 |
C. |
NH3、NO2、CO2 |
D. |
NO、CO2、N2 |
|
下列叙述正确的是 ①海水中含有大量的Br-,所以从海水中提取溴一般要经历浓缩和提取两个步骤 ②铝是一种比较活泼的金属,所以铝合金制品易被腐蚀 ③在炼钢中加入适量的生石灰,可以除去其中的脉石 ④制造玻璃的主要原料是纯碱、石灰石和石英 | |
| [ ] | |
A. |
②③ |
B. |
②④ |
C. |
③④ |
D. |
①③ |
|
等物质的量的SO2和Cl2混合后,缓慢加入BaCl2溶液,再滴入品红试液,发生的现象是 | |
| [ ] | |
A. |
无沉淀生成,溶液显红色 |
B. |
无沉淀生成,溶液显无色 |
C. |
有沉淀生成,溶液显无色 |
D. |
有沉淀生成,溶液显红色 |
|
将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:SO2+2Fe3++2H2O Cr2O | |
| [ ] | |
A. |
还原性Cr3+>Fe2+>SO2 |
B. |
氧化性Cr2O |
C. |
Cr2O |
D. |
两个反应中Fe2(SO4)3均作还原剂 |
|
金属铜的提炼多从黄铜矿开始,已知黄铜矿中铁为+2价.黄铜矿的焙烧过程中主要反应之一的化学方程式为:2CuFeS2+O2 | |
| [ ] | |
A. |
SO2既是氧化产物又是还原产物 |
B. |
CuFeS2既是氧化剂又是还原剂 |
C. |
O2只做氧化剂 |
D. |
若有1 mol O2参加反应,则反应中有4 mol电子转移 |
|
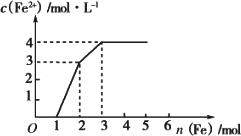
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如下图所示.则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3的物质的量浓度之比为
| |
| [ ] | |
A. |
1∶1∶4 |
B. |
1∶3∶1 |
C. |
3∶3∶8 |
D. |
1∶1∶1 |
|
某溶液中含有①NO | |
| [ ] | |
A. |
① |
B. |
①②④ |
C. |
①③⑤ |
D. |
①④⑤ |
|
下列离子方程式正确的是 | |
| [ ] | |
A. |
氢氧化钡溶液与等物质的量的稀H2SO4混合:Ba2++OH-+H++SO |
B. |
氨气通入醋酸溶液中:CH3COOH+NH3 |
C. |
碳酸氢钙溶液中加入过量的氢氧化钠溶液:HCO |
D. |
澄清石灰水与盐酸反应:H++OH- |