|
有某硫酸和硝酸的混合溶液20 mL,其中含有硫酸的浓度为2 mol/L,含硝酸的浓度为1 mol/L,现向其中加入0.96 g铜粉,充分反应后(假设只生成NO气体),最多可收集到标准状况下的气体的体积为 | |
| [ ] | |
A. |
89.6 mL |
B. |
112 mL |
C. |
168 mL |
D. |
224 mL |
|
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等.下列说法正确的是 | |
| [ ] | |
A. |
元素Y、Z、W离子具有相同的电子层结构,其半径依次增大 |
B. |
元素X与元素Y只能形成一种化合物 |
C. |
元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR |
D. |
元素W、R的最高价氧化物对应水化物都是强酸 |
|
a、b、c、d、e是同周期的五种元素,a和b的最高价氧化物对应水化物呈碱性,且碱性b>a;c和d的气态氢化物的还原性d>c;五种元素的原子得失电子后所形成的简单离子中e的离子半径最小,则它们的原子序数由小到大的顺序是 | |
| [ ] | |
A. |
b、a、d、c、e |
B. |
e、b、a、d、c |
C. |
b、a、e、d、c |
D. |
c、d、e、a、b |
|
有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数).下列说法正确的是 | |
| [ ] | |
A. |
若X(OH)n为强碱,则Y(OH)n也一定为强碱 |
B. |
若HnXOm为强酸,则X的氢化物溶于水一定显酸性 |
C. |
若X元素形成的单质是X2,则Y元素形成的单质一定是Y2 |
D. |
若Y的最高正价为+m,则X的最高正价一定为+m |
|
下列关于元素周期表的说法不正确的是 | |
| [ ] | |
A. |
除零族元素外,非金属元素全部都是主族元素 |
B. |
第三周期非金属元素含氧酸的酸性从左到右依次增强 |
C. |
同周期ⅡA族与ⅢA族元素的原子序数之差可能为25 |
D. |
同族上下相邻两种元素的原子序数之差可能为32 |
|
目前,人类已经发现的非金属元素除稀有气体元素外共有16种,下列对这16种非金属元素的判断不正确的是 ①都是主族元素,原子的最外层电子数都大于3; ②单质在反应中都只能作氧化剂; ③对应的含氧酸都是强酸; ④氢化物常温下都是气态,所以又叫气态氢化物; ⑤气态氧化物与水反应都不会再生成气体 | |
| [ ] | |
A. |
只有①②④⑤ |
B. |
只有①② |
C. |
只有①②③④ |
D. |
全部 |
|
已知短周期元素的离子aA3+,bB+,cC2-,dD-都具有相同的电子层结构,则下列叙述中正确的是 | |
| [ ] | |
A. |
原子半径:A>B>D>C |
B. |
原子序数:d>c>b>a |
C. |
离子半径:C>D>B>A |
D. |
单质的还原性:A>B>D>C |
|
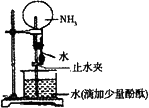
下图是实验室进行氨溶于水的喷泉实验装置,下列叙述不正确的是
| |
| [ ] | |
A. |
该实验说明氨气是一种极易溶于水的气体 |
B. |
进入烧瓶中的液体颜色由无色变为红色,说明氨水有碱性 |
C. |
形成喷泉的原因是氨气溶于水后,烧瓶内的气压小于大气压 |
D. |
用氯气代替氨气,利用此装置也可进行喷泉实验 |
|
原子的核电荷数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数为2n2-1.下列有关X的说法中不正确的是 | |
| [ ] | |
A. |
X能形成化学式为X(OH)3的碱 |
B. |
X能与某些金属元素形成化合物 |
C. |
X原子的最外层电子数和核电荷数肯定为奇数 |
D. |
X可能形成化学式为KXO3的盐 |