|
下列说法不正确的是 | |
| [ ] | |
A. |
Na2CO3比NaHCO3易溶于水 |
B. |
Na2CO3比NaHCO3难分解 |
C. |
溶质的物质的量浓度相同时,NaHCO3溶液比Na2CO3溶液的碱性强 |
D. |
与足量盐酸反应得到相同质量的CO2,所用NaHCO3比Na2CO3的质量要少 |
|
赤铜矿的成份是Cu2O,辉铜矿的成份是Cu2S,将赤铜矿与辉铜矿混合加热有以下反应: 2Cu2O+Cu2S 对于该反应,下列说法中错误的是 | |
| [ ] | |
A. |
反应中铜元素既被氧化又被还原 |
B. |
还原产物与氧化产物的物质的量之比为6∶1 |
C. |
Cu2O在反应中只作氧化剂 |
D. |
反应中被氧化的元素是S |
|
工业生产中物质的循环利用有多种模式,符合下图所示,说法正确的是
| |
| [ ] | |
A. |
可表示工业冶炼镁中的Cl2的循环 |
B. |
可表示电解饱和食盐水中的NaCl的循环 |
C. |
可表示氨氧化法制硝酸中的NO的循环 |
D. |
可表示合成氨中的N2、H2的循环 |
|
根据某元素的原子结构示意图 | |
| [ ] | |
A. |
该原子不如氮原子和硫原子的得电子能力强 |
B. |
该元素形成的单质均很稳定 |
C. |
该元素位于元素周期表的第VA族 |
D. |
该元素最高价氧化物对应的水化物是弱酸 |
|
用NA表示阿伏加德罗常数,下列叙述中正确的是 | |
| [ ] | |
A. |
醋酸的摩尔质量与NA个醋酸分子的质量在数值上肯定不相等 |
B. |
标准状况下,33.6 L H2O中含有1.5NA个H2O分子 |
C. |
标况下,22.4 L氨气所含电子数为7NA |
D. |
1 mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA |
|
下列反应的离子方程式正确的是 | |
| [ ] | |
A. |
用FeCl3溶液腐蚀铜板制印刷电路板:2Fe3++Cu |
B. |
碳酸氢钠的水解:HCO3-+H2O |
C. |
漂白粉溶液中通入过量的CO2:Ca2++2ClO-+CO2+H2O |
D. |
实验室用浓盐酸与 MnO2反应制Cl2:MnO2+2H++2Cl- |
|
下列各项中的两个量,其比值一定为2∶1的是 | |
| [ ] | |
A. |
相同温度下,0.2 mol·L-1醋酸溶液与0.1 mol·L-1醋酸中的c(H+)之比 |
B. |
液面均在“0”刻度时,50 mL碱式滴定管和25 mL碱式滴定管所盛溶液的体积之比 |
C. |
在Na2O2晶体中阳离子与阴离子的物质量之比 |
D. |
22.4 L CO2与22.4 L CO所含氧原子数目之比 |
|
下列关于Cl、N、S等非金属元素化合物的说法正确的是 | |
| [ ] | |
A. |
漂白粉的成分是次氯酸钙 |
B. |
实验室可用浓硫酸干燥氨气 |
C. |
实验室可用NaOH处理NO2和HCl废气 |
D. |
用饱和食盐水吸收氯气的尾气,以达环境保护 |

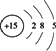 做出如下推理,其中与事实不符的是
做出如下推理,其中与事实不符的是