|
反应 2SO2(g)+O2(g) | |
| [ ] | |
A. |
等于 4 s |
B. |
小于 4 s |
C. |
大于 4 s |
D. |
无法确定 |
|
在不同条件下,四个容器中同时发生如下反应: A(g)+3B(g) | |
| [ ] | |
A. |
v(A)=0.5 mol/(L·s) |
B. |
v(B)=0.6 mol/(L·s) |
C. |
v(C)=0.4 mol/(L·s) |
D. |
v(D)=0.45 mol/(L·s) |
|
已知 4NH3(g)+5O2(g) | |
| [ ] | |
A. |
v(NH3)=v(NO) |
B. |
5v(NH3)=4v(O2) |
C. |
v(NH3)= |
D. |
|
|
反应 4NH3(g)+5O2(g) | |
| [ ] | |
A. |
v(O2)=0.01 mol/(L·s) |
B. |
v(H2O)=0.18 mol/(L·s) |
C. |
v(NO)=0.008 mol/(L·s) |
D. |
v(NH3)=0.002 mol/(L·s) |
|
反应 2SO2+O2 | |
| [ ] | |
A. |
0.1 s |
B. |
2.5 s |
C. |
5 s |
D. |
10 s |
|
不久前,美国一个海军航空站安装了一台 250 kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600~700℃,所用燃料为H2,电解质为熔融的K2CO3,已知该电池的总反应式为:2H2+O2=2H2O,负极反应式为:H2+CO32--2e- | |
| [ ] | |
A. |
该电池的正极反应式为: O2+2H2O+4e- |
B. |
该电池的正极反应式为: 2CO2+O2+4e- |
C. |
电池供应 1 mol水蒸气,转移的电子数为4 mol |
D. |
O2从正极通入,发生氧化反应 |
|
下列说法正确的是 | |
| [ ] | |
A. |
吸热反应一定是需要加热才能发生的反应 |
B. |
伴有能量变化的物质变化都是化学变化 |
C. |
反应是放热还是吸热,必须看反应物和生成物所具有的总能量的相对大小 |
D. |
在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 |
|
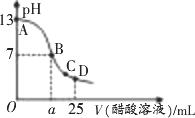
在 25 mL 0.1 mol/L NaOH溶液中逐滴加入0.2 mol/L CH3COOH溶液,曲线如图所示,有关粒子浓度关系正确的是
| |
| [ ] | |
A. |
在 A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
B. |
在 B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+) |
C. |
在 C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
D. |
在 D点:c(CH3COO-)+c(CH3COOH)=2c(Na+)+c(H+) |
|
已知:在 pH值为4左右的环境中,Ca2+、Fe2+几乎不水解,而Fe3+几乎完全水解.工业上制CuCl2是将浓盐酸用蒸气加热到80℃左右,再慢慢加入粗氧化铜(含少量杂质FeO),充分搅拌使之溶解.欲除去溶液中的杂质离子,下述方法中可行的是 | |
| [ ] | |
A. |
加入纯 Cu将Fe2+还原为Fe |
B. |
向溶液中通入 H2S使Fe2+沉淀 |
C. |
向溶液中通入 Cl2,再通入NH3,调节pH值为4左右 |
D. |
向溶液中通入 Cl2,再加入纯净的CuO粉末,调节pH值为4左右 |