|
(创新)在恒容的密闭容器中充入2 mol A和1 mol B,反应2A(g)+B(g) | |
| [ ] | |
A. |
1 |
B. |
2 |
C. |
3 |
D. |
4 |
|
有一可逆反应 mA(g)+nB(g)
| |
| [ ] | |
A. |
正反应吸热, m+n>p+q |
B. |
正反应吸热, m+n<p+q |
C. |
正反应放热, m+n>p+q |
D. |
正反应放热, m+n<p+q |
|
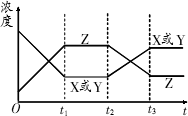
如图所示,反应 X(g)+Y(g)
| |
| [ ] | |
A. |
增大了 X或Y的浓度 |
B. |
使用了催化剂 |
C. |
增大了体系压强 |
D. |
升高了该反应的温度 |
|
下列说法错误的是 | |
| [ ] | |
A. |
NH4NO3溶于水吸热,说明其溶于水不是自发过程 |
B. |
同一种物质气态时熵值最大,液态时次之,固态时熵值最小 |
C. |
借助于外力能自发进行的过程,其体系的能量趋向于从高能态转变为低能态 |
D. |
由焓判据和熵判据组合而成的复合判据,更适合于所有过程自发性的判断 |
|
在固定容积的密闭容器内,加入 2 mol A、1 mol B,发生反应A(g)+B(g) | |
| [ ] | |
A. |
2 mol C |
B. |
3 mol C |
C. |
4 mol A、2 mol C |
D. |
1 mol A、2 mol C |
|
对于平衡体系 aA(g)+bB(g) | |
| [ ] | |
A. |
若温度不变,容器体积扩大一倍,此时 A的浓度是原来的0.48倍,则a+b大于c+d |
B. |
若从正反应开始达到平衡时 A、B的转化率相等,则A、B的起始浓度比为a∶b |
C. |
若平衡体系中共有气体 n mol,再向其中充入b mol B,达到平衡时气体总物质的量为(n+b)mol,则a+b=c+d |
D. |
恒容时,向容器中通入与反应无关的气体,平衡不移动 |
|
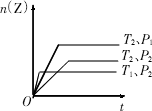
对于反应 2X(g)+Y(g)
| |
| [ ] | |
A. |
T1<T2,P1<P2,正反应为放热反应 |
B. |
T1<T2,P1>P2,正反应为吸热反应 |
C. |
T1>T2,P1>P2,正反应为放热反应 |
D. |
T1>T2,P1<P2,正反应为吸热反应 |
|
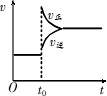
往一体积不变的密闭容器中充入 H2和I2,反应H2(g)+I2(g) | |
| [ ] | |
A. |
容器内气体颜色变深,平均相对分子质量不变 |
B. |
平衡不移动,混合气体的密度增大 |
C. |
H2的转化率增大,HI的平衡浓度变小 |
D. |
改变条件前后,速率图象如图所示
|
|
恒温时,一恒压容器内发生反应 2NO2(g) | |
| [ ] | |
A. |
不变 |
B. |
增大 |
C. |
减小 |
D. |
无法判断 |
|
常温下,在一支注射器内,吸入一定体积的 NO2,当达到平衡(原平衡)时,将注射器的活塞迅速向内压至某一位置,红棕色先突然变深后又逐渐变浅,最终达到新的化学平衡.则原平衡与新平衡相比,NO2气体的浓度 | |
| [ ] | |
A. |
前者大 |
B. |
后者大 |
C. |
相等 |
D. |
都有可能 |