|
某一温度下,在一密闭容器中,起始充入一定量的 C(s)、H2O(g)、CO(g)和H2(g),反应C(s)+H2O(g) | |
| [ ] | |
A. |
一定变大 |
B. |
一定变小 |
C. |
一定不变 |
D. |
变大、变小、不变都有可能 |
|
下列关于化学反应熵变的叙述,正确的是 | |
| [ ] | |
A. |
化学反应的熵变与反应的方向无关 |
B. |
化学反应的熵变直接决定了反应进行的方向 |
C. |
熵增大的反应都是混乱度增大的反应 |
D. |
自发进行的反应一定是熵增加的反应 |
|
实验证明,多数能自发进行的反应都是放热反应.对此说法理解正确的是 | |
| [ ] | |
A. |
所有的放热反应都是自发进行的 |
B. |
所有的自发反应都是放热的 |
C. |
焓变是影响反应是否具有自发性的一种重要因素 |
D. |
焓变是决定反应是否具有自发性的唯一判据 |
|
碳酸铵在室温下就能自发地分解产生氨气,下列对其说法正确的是 | |
| [ ] | |
A. |
碳酸铵分解是因为生成了易挥发的气体,使体系的熵增大 |
B. |
碳酸铵分解是因为外界给予了能量 |
C. |
碳酸铵分解是吸热反应,根据焓判据可知该反应不能自发进行 |
D. |
碳酸盐都不稳定,都能自发分解 |
|
在恒温、恒压条件下,向容积可变的密闭容器中充入 3 mol A和2 mol B,发生如下反应:3A(g)+2B(g)m%,则x、y的值分别为 | |
| [ ] | |
A. |
x=3、y=1 |
B. |
x=4、y=1 |
C. |
x=5、y=1 |
D. |
x=10、y=3 |
|
可逆反应 A(g)+B(g) | |
| [ ] | |
A. |
m>n |
B. |
m<n |
C. |
m=n |
D. |
无法比较 |
|
在一定温度时,将 2 mol SO2和1 mol O2置于一恒容密闭容器中,发生反应2SO2(g)+O2(g) | |
| [ ] | |
A. |
2、2、0 |
B. |
2、1、2 |
C. |
0、0、2 |
D. |
2、1.5、2 |
|
在一个恒容的密闭容器内,充入 10 mol N2和30 mol H2,发生合成氨反应N2+3H2 | |
| [ ] | |
A. |
15 mol 25% |
B. |
20 mol 50% |
C. |
20 mol 75% |
D. |
40 mol 80% |
|
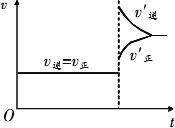
下图所示为某反应物的速率-时间图,下列对该反应的推测合理的是
| |
| [ ] | |
A. |
增大压强对正反应是气体体积减小的可逆反应平衡体系的影响 |
B. |
升高温度对正反应吸热的可逆反应平衡体系的影响 |
C. |
减小生成物浓度对可逆反应平衡体系的影响 |
D. |
升高温度对正反应放热的可逆反应平衡体系的影响 |