|
一定能在下列溶液中大量共存的离子组是 | |
| [ ] | |
A. |
c(H+)=1×10-13 mol·L-1的溶液:Na+、Ca2+、SO42-、CO32- |
B. |
含有大量Fe3+的溶液:Na+、Mg2+、NO3、SCN- |
C. |
含大量Al3+的溶液:Na+、NH4+、SO42-、Cl- |
D. |
含有大量NO3-的溶液:H+、Fe2+、SO42-、Cl- |
|
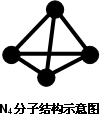
意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1 mol N-N键吸收167 kJ热量,生成1 mol N≡N键放出942 kJ热量.下列叙述正确的是
| |
| [ ] | |
A. |
N4属于一种新型的化合物 |
B. |
N4与N2互为同素异形体 |
C. |
N4沸点比P4(白磷)高 |
D. |
1 mol N4气体转变为N2吸收882 kJ热量 |
|
如图是课外活动小组的同学设计的4个喷泉实验方案.下列有关操作不可能引发喷泉现象的是
| |
| [ ] | |
A. |
挤压装置①的胶头滴管使CCl4全部进入烧瓶,片刻后打开止水夹 |
B. |
挤压装置②的胶头滴管使NaOH溶液全部进入烧瓶,片刻后打开止水夹 |
C. |
打开装置③的a处开关,并打开止水夹,用鼓气装置从a处不断鼓入空气 |
D. |
打开止水夹,向装置④的水槽中慢慢加入足量浓硫酸 |
|
下列说法中错误的是 | |
| [ ] | |
A. |
干冰与二氧化硅晶体熔化时,所克服的微粒间相互作用不相同 |
B. |
C2H5OH与C2H5Br相比,前者的相对分子质量远小于后者,而沸点却远高于后者,其原因是前者的分子间存在氢键 |
C. |
非金属单质只能形成分子晶体 |
D. |
短周期元素离子aXm-和bYn-具有相同的电子层结构,若a>b,则n>m |
|
下列实验方案合理的是 | |
| [ ] | |
A. |
用湿润的pH试纸测定某盐溶液的pH |
B. |
用稀硫酸清洗长期存放氯化铁溶液的试剂瓶内壁所附着的不溶物 |
C. |
用加热法分离I2和NH4Cl的混合物 |
D. |
为了更快得到氢气,可以用纯锌代替粗锌与稀硫酸反应 |
|
已知SO2(g)+1/2O2(g) | |
| [ ] | |
A. |
该条件下加入2 mol SO2与1 mol O2充分反应,放出热量为196.0 kJ |
B. |
若不加入催化剂,ΔH将不等于-98.0 kJ/mol |
C. |
升高温度平衡向逆反应方向移动 |
D. |
工业生产中采取增大压强的方法,提高SO2的转化率 |
|
下列除杂方法中,正确的是 | |
| [ ] | |
A. |
用灼烧法除去二氧化锰中混有的炭粉 |
B. |
用点燃法除去CO2中混有的少量CO |
C. |
将H2和O2混和气体通过灼热的CuO以除去氧气中的氢气 |
D. |
干燥H2S中的水蒸气,将混和气通过浓硫酸的洗气瓶 |
|
下列反应的离子方程式错误的是 | |
| [ ] | |
A. |
足量的CO2通入饱和碳酸钠溶液中:CO2+2Na++CO32-+H2O=2NaHCO3↓ |
B. |
氢氧化铁与足量的氢溴酸溶液反应:Fe(OH)3+3H+=Fe3++3H2O |
C. |
等物质的量的Ba(OH)2与NH4HSO4在稀溶液中反应: Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
D. |
向碳酸氢钠溶液中滴入少量澄清石灰水: Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O |
|
下列说法错误的是 ①测定中和热时,为了减少热量损失,不要搅拌溶液 ②银镜反应实验后的试管可用稀氨水洗涤 ③向氯化铁溶液里滴入氢氧化钠溶液可以制取氢氧化铁胶体 ④SO2气体通入溴水,溴水褪色,说明SO2有漂白性 ⑤向含有乙酸杂质的乙酸乙酯中加入氢氧化钠溶液后分液,提纯乙酸乙酯 | |
| [ ] | |
A. |
①②④⑤ |
B. |
①②③ |
C. |
②③④ |
D. |
全部 |