|
化学与人们的生活、健康密切相关.下列做法不合理的是: | |
| [ ] | |
A. |
用米汤检验加碘食盐中的碘酸钾(KIO3) |
B. |
向豆浆中加入盐卤(主要成分为MgCl2)制做豆腐 |
C. |
用灼烧和闻气味的方法区别棉织物和纯毛织物 |
D. |
用透析的手段净化尿毒症患者的血液 |
|
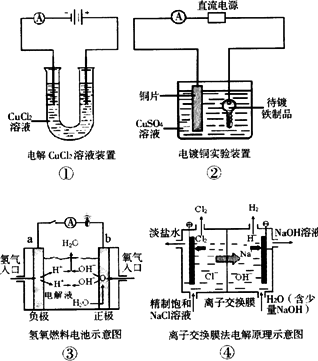
关于下列各图的说法,正确的是
| |
| [ ] | |
A. |
①装置中阴极处产生的气体能够使湿润淀粉KI试纸变蓝 |
B. |
②装置中待镀铁制品应与电源正极相连 |
C. |
③装置中电子由b极流向a极 |
D. |
④装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |
|
元素X、Y和Z可结合形成化合物XYZ3;X、Y和Z的原子序数之和为26;Y和Z在同一周期.下列有关推测正确的是 | |
| [ ] | |
A. |
XYZ3是一种可溶于水的酸,且X与Y可形成分子晶体XY |
B. |
XYZ3是一种微溶于水的盐,且X与Z可形成离子晶体XZ |
C. |
XYZ3是一种易溶于水的盐,且Y与Z可形成离子晶体YZ |
D. |
XYZ3是一种离子化合物,且Y与Z可形成离子晶体YZ3 |
|
如图所示,a、b、c均为石墨电极,d为碳钢电极,通电进行电解.假设在电解过程中产生的气体全部逸出,下列说法正确的是
| |
| [ ] | |
A. |
甲、乙两烧杯中溶液的pH均保持不变 |
B. |
甲烧杯中a的电极反应式为4OH――4e-=O2↑+2H2O |
C. |
当电解一段时间后,将甲乙两溶液混合,一定会产生蓝色沉淀 |
D. |
当b极增重3.2 g时,d极产生的气体为2.24 L(标准状况) |
|
如果取一块冰放在容器里,不断地升高温度,可以实现“冰→水→水蒸气→氢气和氧气”的变化,在各步变化时破坏的粒子间的相互作用依次是 | |
| [ ] | |
A. |
氢键、极性键、非极性键 |
B. |
氢键、氢键、极性键 |
C. |
氢键、氢键、非极性键 |
D. |
氢键、非极性键、极性键 |
|
用惰性电极电解CuSO4溶液,一段时间后取出电极.向电解后的溶液中加入9.8 g的Cu(OH)2,充分反应后所得溶液与电解前相同,则电解时电路中通过电子的物质的量是 | |
| [ ] | |
A. |
0.4 mol |
B. |
0.3 mol |
C. |
0.2 mol |
D. |
0.1 mol |
|
下列离子方程式正确的是 | |
| [ ] | |
A. |
甲酸钠溶液和盐酸反应:HCOO-+H+ |
B. |
次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO |
C. |
常温下Al与浓硝酸反应:Al+6H++3NO3-=Al3++3NO2↑+3H2O |
D. |
澄清石灰水与少量苏打溶液混合:Ca2++OH-+HCO3-=CaCO3↓+H2O |
|
下列叙述正确的是 | |
| [ ] | |
A. |
测定中和热时,为了减少热量损失,不要搅拌溶液. |
B. |
为测定硫酸铜晶体的结晶水含量,称样时,应先称取一定量的晶体,后放入坩埚. |
C. |
在中学“硫酸铜晶体中结晶水含量测定”的实验中称量操作最多需要四次. |
D. |
测定中和热实验可以在保温瓶中进行. |