|
现有如下各说法: ①在水中氢、氧原子间均以化学键相结合. ②金属与非金属化合一定形成离子键. ③离子键是阳离子、阴离子的相互吸引. ④根据电离方程式:HCl ⑤H2和Cl2的反应过程是H2、Cl2分子中共价键发生断裂生成H、Cl原子,然后H、Cl原子形成离子键的过程. 上述各种说法正确的是 | |
| [ ] | |
A. |
①②⑤正确 |
B. |
都不正确 |
C. |
④正确,其他不正确 |
D. |
仅①不正确 |
|
A+、A2+、C-、D2-四种主族元素的离子具有相同的电子层结构.现有以下排列顺序:①B2+>A+>C->D2-;②C->D2->A+>B2+;③B2+>A+>D2->C-;④D2->C->A+>B2+.四种离子的半径由大到小以及四种元素原子序数由大到小的顺序分别是 | |
| [ ] | |
A. |
①④ |
B. |
④① |
C. |
②③ |
D. |
③② |
|
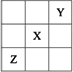
已知X、Y、Z三种主族元素在周期表中的相对位置如图所示,且X的原子序数为a,下列说法不正确的是
| |
| [ ] | |
A. |
Y、Z的原子序数之和可能为2a |
B. |
Y的原子序数可能是a-17 |
C. |
Z的原子序数可能是a+31 |
D. |
X、Y、Z一定都是短周期元素 |
|
现有X、Y、Z三种短周期元素,X、Y为相邻周期,X的质子数比Y少5,X的最外层电子数是Y的2倍,Y与Z的最外层电子数之差为3.它们组成的物质的化学式不正确的是 | |
| [ ] | |
A. |
Y2ZY3 |
B. |
Y2(ZX4)3 |
C. |
Y2X3 |
D. |
Y2Z3 |
|
运用元素周期律分析下面的推断,其中错误的是 | |
| [ ] | |
A. |
铍的氧化物的水化物可能具有两性 |
B. |
硫酸锶是难溶于水的白色固体 |
C. |
砹为有色固体,HAt不稳定,AgAt感光性很强,但不溶于水也不溶于稀酸 |
D. |
硒化氢是无色、有毒、比硫化氢稳定的气体 |