|
H2是一种很有前途的能源,以水为原料大量制取H2,最理想的途径是 | |
| [ ] | |
A. |
利用太阳能直接使水分解为H2 |
B. |
以焦炭和水为原料制水煤气后再分离出H2 |
C. |
以赤热的Fe和水反应生成H2 |
D. |
由热电厂提供电能,利用直流电电解水产生H2 |
|
已知化学反应2C(s)+O2(g) | |
| [ ] | |
A. |
12 g C所具有的能量一定高于28 g CO所具有的能量 |
B. |
56 g CO和32 g O2所具有的总能量大于44 g CO2所具有的总能量 |
C. |
12 g C和32 g O2所具有的总能量大于44 g CO2所具有的总能量 |
D. |
将一定质量的C燃烧,生成CO2比生成CO时放出的热量多 |
|
氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车备受青睐.我国拥有完全自主知识产权的氢燃料电池轿车“超越三号”,已达到世界先进水平,正在加快向产业化的目标迈进.氢能具有的优点包括 ①原料来源广 ②易燃烧、热值高 ③储存方便 ④制备工艺廉价易行 | |
| [ ] | |
A. |
①② |
B. |
①③ |
C. |
③④ |
D. |
②④ |
|
铅蓄电池用途极广,可多次充放电.铅蓄电池中铅作负极,二氧化铅作正极,电解液为30%的H2SO4溶液.电池充、放电时的总反应可表示为: Pb+PbO2+2H2SO4 下列关于此电池的说法中,不正确的是 | |
| [ ] | |
A. |
放电一段时间后,电解液的pH将增大 |
B. |
放电时,铅电极上发生的电极反应式为:Pb+ |
C. |
充电时,二氧化铅电极上发生氧化反应 |
D. |
充电时,电解液中的阳离子向二氧化铅极移动 |
|
目前常用的镍(Ni)镉(Cd)电池,其电池总反应式可表示为: Cd+2NiO(OH)+2H2O | |
| [ ] | |
A. |
以上反应是可逆反应 |
B. |
该废弃电池在酸性土壤中的污染尤为严重 |
C. |
充电时化学能转变成电能 |
D. |
放电时的负极材料是Ni(OH)2 |
|
蓄电池在放电时起原电池的作用,在充电时起电解池的作用.下式是爱迪生蓄电池分别在充电和放电时发生的反应: Fe+NiO2+2H2O 下列有关该蓄电池的推断不正确的是 | |
| [ ] | |
A. |
放电时Fe是负极,NiO2是正极 |
B. |
放电时正极反应是:NiO2+H2O+2e- |
C. |
放电时,电解质溶液中阴离子向正极方向移动 |
D. |
蓄电池的电极必须浸入某种碱性电解质溶液中 |
|
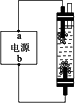
某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,设计了如图的装置,则对电源电极名称和消毒液的主要成分判断正确的是
| |
| [ ] | |
A. |
a为正极,b为负极;NaClO和NaCl |
B. |
a为负极,b为正极;NaClO和NaCl |
C. |
a为阳极,b为阴极;HClO和NaCl |
D. |
a为阴极,b为阳极;HClO和NaCl |
|
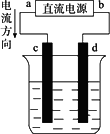
下图是电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是
| |
| [ ] | |
A. |
a为负极,b为正极 |
B. |
a为阳极,b为阴极 |
C. |
电解过程中,d电极质量增加 |
D. |
电解过程中,氯离子浓度不变 |
|
关于电解NaCl水溶液,下列叙述正确的是 | |
| [ ] | |
A. |
电解时在阳极得到氯气,在阴极得到金属钠 |
B. |
若在阳极附近的溶液中滴入KI溶液,溶液呈棕色 |
C. |
若在阴极附近的溶液中滴入酚酞试液,溶液呈无色 |
D. |
电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性 |