|
在100 g浓度为18 mol·L-1、密度为ρ的浓硫酸中加入一定量的水稀释成9 mol·L-1的硫酸,则加入水的体积( ). | |
| [ ] | |
A. |
小于100 mL |
B. |
等于100 mL |
C. |
大于100 mL |
D. |
等于 |
|
已知98%的浓硫酸的浓度为18.4 mol·L-1,则49%的硫酸溶液的浓度( ). | |
| [ ] | |
A. |
等于9.2 mol·L-1 |
B. |
大于9.2 mol·L-1 |
C. |
小于9.2 mol·L-1 |
D. |
不能确定 |
|
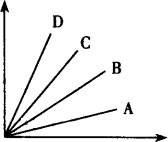
将钠、镁、铝、铁四种金属分别跟足量的硫磺反应,消耗硫磺的质量(横坐标)与生成金属硫化物的质量(纵坐标)如图所示(A、B、C、D分别表示一种金属与硫磺反应的上述质量关系).
则这四种金属按A、B、C、D的顺序排列为( ). | |
| [ ] | |
A. |
Na、Mg、Al、Fe |
B. |
Fe、Al、Mg、Na |
C. |
Al、Mg、Na、Fe |
D. |
Mg、Al、Na、Fe |
|
硫元素的非金属性弱于氯元素的事实是( ). | |
| [ ] | |
A. |
通常情况下,硫为浅黄色固体,而氯气为黄绿色气体 |
B. |
硫不溶于水,而氯气溶于水 |
C. |
跟金属或H2反应时,硫被还原为-2价,而氯被还原为-1价 |
D. |
跟同一金属(如Cu或Fe)反应时,金属被硫氧化成低价态,而金属却被氯氧化成高价态 |
|
在硫酸的工业制法中,下列生产操作与说明生产操作的主要原因二者都正确的是( ). | |
| [ ] | |
A. |
硫铁矿燃烧前要粉碎,因为大块硫铁矿不能燃烧 |
B. |
从沸腾炉出来的气体需净化,因为炉气中的SO2会与杂质反应 |
C. |
SO2氧化成SO3,SO2能全部转化为SO3 |
D. |
SO3用98.3%的浓H2SO4吸收,目的是防止形成酸雾,以便使SO3吸收完全 |
|
向50 mL 18 mol·L-1 H2SO4溶液中加入足量的铜片并加热.充分反应后,被还原的H2SO4的物质的量( ). | |
| [ ] | |
A. |
小于0.45 mol |
B. |
等于0.45 mol |
C. |
在0.45 mol和0.90 mol之间 |
D. |
大于0.90 mol |