|
银锌电池广泛用作各种电子仪器的电源,它的放电过程可表示为: Ag2O+Zn+H2O 此电池放电时,负极上发生反应的物质是 | |
| [ ] | |
A. |
Ag |
B. |
Zn(OH)2 |
C. |
Ag2O |
D. |
Zn |
|
X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,X与Y组成原电池时,Y为电池的负极.X、Y、Z三种金属的活动性顺序为 | |
| [ ] | |
A. |
X>Y>Z |
B. |
X>Z>Y |
C. |
Y>X>Z |
D. |
Y>Z>X |
|
下列说法正确的是 | |
| [ ] | |
A. |
通常条件下,吸热反应不能自发进行 |
B. |
放热反应必须在加热条件下才能进行 |
C. |
放热反应一旦发生就可继续进行下去 |
D. |
由原子结合形成1 mol化学键放出的能量越多,该化学键就越稳定 |
|
1 g氢气燃烧生成液态水放出142.9 kJ热量,表示该反应的热化学方程式正确的是 | |
| [ ] | |
A. |
2H2(g)+O2(g) |
B. |
2H2(g)+O2(g) |
C. |
2H2+O2 |
D. |
2H2(g)+O2(g) |
|
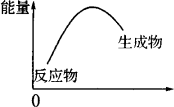
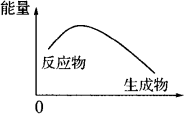
关于吸热反应和放热反应,下列说法中错误的是 | |
| [ ] | |
A. |
需要加热才能进行的化学反应一定是吸热反应 |
B. |
化学反应过程中的能量变化,除了热量外,还可以是光能、电能 |
C. |
化学反应过程中的能量变化,也服从能量守恒定律 |
D. |
反应物的总能量高于生成物的总能量时,发生放热反应 |
|
1 mol N2H4(g)在适量的O2(g)中燃烧,生成N2(g)和H2O(g),放出534 kJ的热量,则相同条件下,下列判断正确的是 | |
| [ ] | |
A. |
1 mol N2H4(g)的能量比1 mol N2(g)能量高534 kJ |
B. |
1 mol N2H4(g)的能量比1 mol N2(g)能量低534 kJ |
C. |
1 mol N2H4(g)和1 mol O2的总能量比1 mol N2(g)和2 mol H2O(g)的总能量高534 kJ |
D. |
1 mol N2H4(g)和1 mol O2的总能量比1 mol N2(g)和2 mol H2O(g)的总能量低534 kJ |