|
用物质的量都是0.1 mol的CH3COOH和CH3COONa混合后配成1 L溶液,已知溶液中的c(CH3COO-)>c(Na+),下列关系正确的是 | |
| [ ] | |
A. |
c(H+)<c(OH-) |
B. |
c(CH3COOH)>c(CH3COO-) |
C. |
c(CH3COO-)+c(OH-)=0.1 mol?L-1 |
D. |
c(CH3COOH)+c(CH3COO-)=0.2 mol?L-1 |
|
常温时,纯水中由水电离的c(H+)=a,pH=1的盐酸中由水电离的c(H+)=b,0.2 mol?L-1的盐酸与0.1 mol?L-1的氢氧化钠溶液等体积混合后,由水电离的c(H+)=c,则a、b、c的关系正确的是 | |
| [ ] | |
A. |
a>b=c |
B. |
a>c>b |
C. |
c>b>a |
D. |
b>c>a |
|
人体血液的正常pH约为7.35~7.45,若在外界因素作用下pH突然发生较大的改变就会引起“酸中毒”或“碱中毒”,甚至有生命危险.由于人体体液的缓冲系统中存在如下平衡: H++HCO3- H++PO43- H++HPO42- 故能维持血液pH的相对稳定,以保证正常生理活动.下列说法中不合理的是 | |
| [ ] | |
A. |
当强酸性物质进入人体的体液后,上述缓冲系统的平衡向右移,从而维持pH稳定 |
B. |
当强碱性物质进入人体的体液后,上述缓冲系统的平衡向左移,从而维持pH稳定 |
C. |
某病人在静脉滴注大量生理盐水后,血液被稀释,会导致c(H+)显著减少,pH值显著增大,可能会引起碱中毒 |
D. |
在人体进行正常呼吸活动时,CO2进入血液,会使平衡向左移动,c(H+)略增大,pH值改变很小 |
|
下列各溶液中,微粒的物质的量浓度关系正确的是 | |
| [ ] | |
A. |
10 mL 0.5 mol/L CH3COONa溶液与6 mL 1 mol/L盐酸混合: c(Cl-)>c(Na+)>c(OH-)>c(H+) |
B. |
c(NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液以及(NH4)2Fe(SO4)2溶液: C[(NH4)2Fe(SO4)2]<c[(NH4)2SO4]<c[(NH4)2CO3] |
C. |
0.1 mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) |
D. |
在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-) |
|
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.该电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“-”.高铁电池的总反应为: 3Zn+2K2FeO4+8H2O 下列叙述不正确的是 | |
| [ ] | |
A. |
放电时正极反应为: |
B. |
充电时阴极反应为:Zn(OH)2+2e-=Zn+2OH- |
C. |
放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化 |
D. |
标有“+”的接线柱充电时作阳极,放电时作正极 |
|
已知同温度下的溶解度:Zn(OH)2>ZnS,MgCO3>Mg(OH)2;就溶解或电离出S2-的能力而言,FeS>H2S>CuS,则下列离子方程式错误的是 | |
| [ ] | |
A. |
Mg2++2HCO3-+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O |
B. |
Cu2++H2S=CuS↓+2H+ |
C. |
Zn2++S2-+2H2O=Zn(OH)2↓+H2S↑ |
D. |
FeS+2H+=Fe2++H2S↑ |
|
已知在pH为4~5的环境中,Cu2+、Fe2+几乎不水解,而Fe3+几乎完全水解.工业上制CuCl2是将浓盐酸用蒸气加热到80℃左右,再慢慢加入粗氧化铜(含少量杂质FeO),充分搅拌使之溶解.欲除去溶液中的杂质离子,下述方法中可行的是 | |
| [ ] | |
A. |
加入纯NaClO固体,调节pH值为4~5 |
B. |
向溶液中通入H2S使Fe2+沉淀 |
C. |
向溶液中通入Cl2,再通入NH3,调节pH值为4~5 |
D. |
向溶液中通入Cl2,再加入纯净的CuO粉末调节pH值为4~5 |
|
pH值相同的四种一元酸A、B、C、D的溶液各20 mL,与过量Mg充分反应后,产生氢气的质量是D>C>A=B.下列说法正确的是: ①D的酸性最强 ②A与B的酸性最强且彼此相当 ③反应后原D溶液的PH最大 ④反应后原A和B溶液的PH最大 ⑤反应前D溶液的物质的量浓度最大 ⑥反应前四种溶液物质的量浓度一样大 | |
| [ ] | |
A. |
②③⑤ |
B. |
①④⑥ |
C. |
②④⑤ |
D. |
①③⑤ |
|
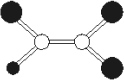
如图是某种有机物分子的球棍模型图.图中的“棍”代表单键或双键,不同大小的“球”代表三种不同的短周期元素的原子.对该有机物的叙述不正确的是
| |
| [ ] | |
A. |
该有机物可能的分子式为C2HCl3 |
B. |
该有机物分子中一定有C=C键 |
C. |
该有机物分子中的所有原子在同一平面上 |
D. |
该有机物可以由乙炔和氯化氢加成反应得到 |
|
100℃时,将0.1 mol N2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) 下列结论不能说明上述反应在该条件下已经达到平衡状态的是 ①烧瓶内气体的颜色不再加深,②N2O4消耗速率与NO2生成速率之比为1∶2,③NO2的生成速率与NO2的消耗速率相等,④NO2的物质的量浓度不变,⑤烧瓶内气体的质量不再变化,⑥烧瓶内气体的压强不再变化,⑦烧瓶内气体的密度不再变化,⑧烧瓶内气体的平均相对分子质量不再变化 | |
| [ ] | |
A. |
②⑤ |
B. |
⑤⑦⑧ |
C. |
②⑤⑦ |
D. |
①③④⑥⑧ |