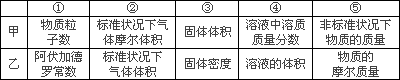
|
已知A、B、C、D均位于前3周期,且aA2+、bB+、cC3-、dD-核外电子层结构完全相同.则下列有关叙述正确的是 | |
| [ ] | |
A. |
原子半径A>B>D>C |
B. |
原子序数d>c>b>a |
C. |
离子半径C>D>B>A |
D. |
单质的还原性A>B>D>C |
|
下列说法正确的是 | |
| [ ] | |
A. |
在101 kPa时,1 mol C与适量O2反应生成1 mol CO时,放出110.5 kJ热量,则C的燃烧热为110.5 kJ/mol |
B. |
在101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量,则H2的燃烧热为-285.8 kJ/mol |
C. |
测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度、NaOH起始温度和反应后终止温度 |
D. |
在稀溶液中:H+(aq)+OH-(aq) |
|
在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度和气体密度相等时,下列说法正确的是: | |
| [ ] | |
A. |
两种气体的压强相等 |
B. |
O2比O3质量小 |
C. |
两种气体的分子数目相等 |
D. |
两种气体的氧原子数目相等 |
|
常温下,某溶液中由水电离出来的c(H+)=1.0×10-13 mol·L-1,该溶液可能是 ①二氧化硫 ②氯化铵水溶液 ③硝酸钠水溶液 ④氢氧化钠水溶液 | |
| [ ] | |
A. |
①④ |
B. |
①② |
C. |
②③ |
D. |
③④ |
|
下列叙述正确的是 | |
| [ ] | |
A. |
金属与盐溶液反应都是置换反应 |
B. |
阴离子都只有还原性 |
C. |
与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物 |
D. |
分子晶体中都存在范德瓦尔斯力,可能不存在共价键 |
|
根据中学化学教材所附元素周期表判断,下列叙述正确的是 | |
| [ ] | |
A. |
L电子层电子数为奇数的所有元素都是非金属 |
B. |
第三、四、五、六周期元素的数目分别是8、18、32、32 |
C. |
由左至右第8、9、10三列元素中没有非金属元素 |
D. |
只有第ⅡA族元素的原子最外层有2个电子 |
|
下列有关结构和性质的说法中,正确的是 | |
| [ ] | |
A. |
酸性:HCl>H2S,所以非金属性:Cl>S |
B. |
同周期(除0族)元素原子的最外层电子数越多,越容易得电子,非金属性越强 |
C. |
NH3、HNO3都是电解质二者反应后的产物是 离子化合物,含极性共价键和离子键 |
D. |
原子核外最外层电子数与最内层电子数相等的元素一定是金属元素 |