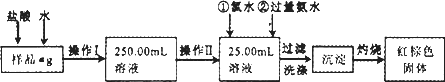
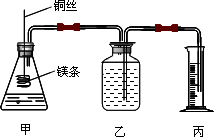
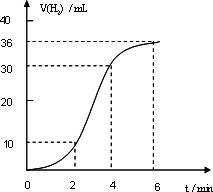
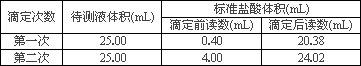
0 88290 88298 88304 88308 88314 88316 88320 88326 88328 88334 88340 88344 88346 88350 88356 88358 88364 88368 88370 88374 88376 88380 88382 88384 88385 88386 88388 88389 88390 88392 88394 88398 88400 88404 88406 88410 88416 88418 88424 88428 88430 88434 88440 88446 88448 88454 88458 88460 88466 88470 88476 88484 203614