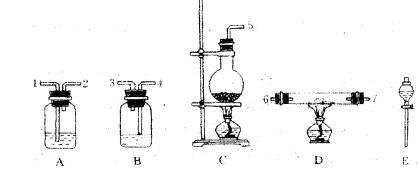
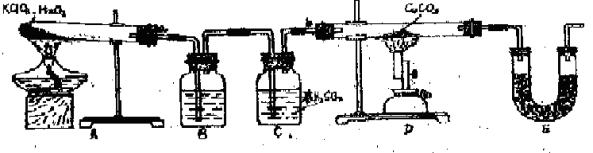
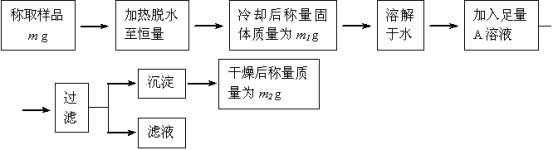
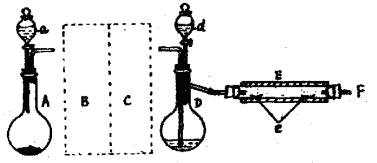
已知下列数据:
|
物质 |
熔点代 |
沸点/℃ |
密度/·cm-3 |
|
乙醇 |
-144 |
78 |
0.789 |
|
乙酸 |
16.6 |
117.9 |
1.05 |
|
乙酸乙酯 |
-83.6 |
77.5 |
0.900 |
|
浓H2SO4 |
|
338 |
1.84 |
实验室制乙酸乙酯的主要装置如下图(a)所示,主要步骤为:①在30mL的大试管中按体积比1:4:4的比例配制浓硫酸、乙醇和乙酸的混合液;②按(a)图连接装置,使产生的蒸气经导管通到15ml试管所盛饱和Na2CO3溶液(加入1滴酚酞试液)上方2mm~3mm处;③小火加热试管中的混合液;①待小试管中收集到约4mL产物时停止加热,撤出小试管并用力振荡,然后静置待其分层;⑤分离出纯净的乙酸乙酯。
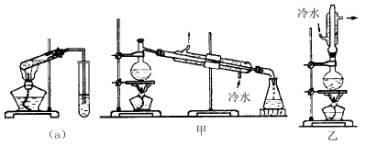
请回答下列问题:
(1)步骤①中,配制这一比例的混合液的操作是___________________。
(2)写出该反应的化学方程式________,浓H2SO4的作用是________。
(3)步骤③中,用小火加热试管中的混合液,其原因是________。
(4)步骤④所观察到的现象是________,写出原因与结论:________。
(5)步骤⑤中,分离出乙酸乙酯选用的仪器是________,产物应从________口倒出,因为________。
(6)为提高乙酸乙酯的产率,甲、乙两位同学分别设计了如上图甲、乙的装置(乙同学待反应完毕冷却后再用饱和Na2CO3溶液提取烧瓶中产物)。你认为哪种装置合理,为什么?答________。
经测定乙醇的分子式是C2H6O。由于有机化合物普遍存在同分异构现象,推测乙醇结构可能是下列两种之一:
(Ⅰ)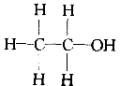 (Ⅱ)
(Ⅱ)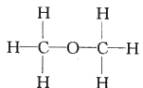 为确定其结构,应利用物质的特殊性质进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,请甲、乙、丙、丁四名学生直接利用如图给定的装置开始进行实验确定乙醇的结构。
为确定其结构,应利用物质的特殊性质进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,请甲、乙、丙、丁四名学生直接利用如图给定的装置开始进行实验确定乙醇的结构。
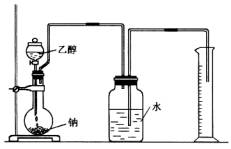
(1)学生甲得到一组实验数据:
|
乙醇的物质的量 |
氢气的体积(标准状况) |
|
0.10mol |
1.12L |
根据以上数据推断乙醇的结构应为________(用Ⅰ、Ⅱ表示),理由是___________。
(2)学生乙分别准确称量4.60 g乙醇进行多次实验,结果发现已排到量筒内的水的体积作为生成氢气的体积换算成标准状况后都小于1.12L。如果忽略量筒本身及读数造成的误差,那么学生乙认为是由于样品乙醇中含有少量水造成的,你认为正确吗?答:__________(填“正确”或“不正确”)。如果你认为正确,请说明理由;你认为不正确,那么产生这种情况的原因应是什么?答________
(3)学生丙认为实验成功的关键有:①装置气密性良好;②实验开始前准确确定乙醇的量;③钠足量;④广口瓶内必须充满水;⑤氢气体积的测算方法正确、数值准确。其中正确的有__________(填序号)。
(4)学生丁不想通过称量乙醇的质量来确定乙醇的量,那么他还需要知道的数据是__________。
(5)实验后四名学生从乙醇的可能结构分析人手对乙醇和钠的量的关系进行讨论,如果乙醇的物质的量为nmol,那么对钠的物质的量的取值要求必须是__________。