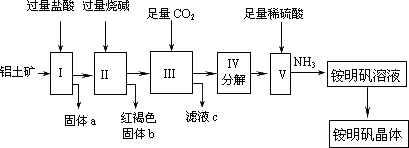
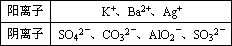0 88184 88192 88198 88202 88208 88210 88214 88220 88222 88228 88234 88238 88240 88244 88250 88252 88258 88262 88264 88268 88270 88274 88276 88278 88279 88280 88282 88283 88284 88286 88288 88292 88294 88298 88300 88304 88310 88312 88318 88322 88324 88328 88334 88340 88342 88348 88352 88354 88360 88364 88370 88378 203614