如图为向盛有0.2 mol•L-1 50 mL明矾溶液中,慢慢加入0.1 mol•L-1
Ba(OH)2溶液,生成沉淀的质量随着加入Ba(OH)2溶液的体积变化的图像,当产生的沉淀量最大时(即B点)改加0.5 mol•L-1
HCl.沉淀总质量又发生变化(虚线部分)。
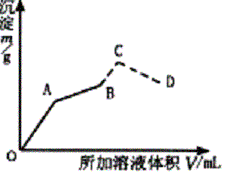
⑴写出OA、AB、C、CD四段发生反应的化学方程式。
⑵计算A、B、C、D点所加入Ba(OH)2溶液、盐酸体积及沉淀质量并填入下表。
|
|
A |
B |
|
V[Ba(OH)2]/mL |
|
|
|
m(沉淀)/g |
|
|
工业上制备氯化铜时,是将浓盐酸有蒸气加热80℃左右,慢慢加入粗制的CuO粉末(含有杂质FeO),用浓盐酸溶解,得到的氯化铜溶液中含有一定量的Fe2+。
0 87293 87301 87307 87311 87317 87319 87323 87329 87331 87337 87343 87347 87349 87353 87359 87361 87367 87371 87373 87377 87379 87383 87385 87387 87388 87389 87391 87392 87393 87395 87397 87401 87403 87407 87409 87413 87419 87421 87427 87431 87433 87437 87443 87449 87451 87457 87461 87463 87469 87473 87479 87487 203614
|
金属离子 |
pH |
|
|
开始沉淀 |
沉淀完全 |
|
|
Fe2+ |
7.6 |
9.6 |
|
Cu2+ |
4.4 |
6.4 |
|
Fe3+ |
2.7 |
3.7 |
⑴从上表提供的数据看,不能直接将溶液的PH调到9.6除去Fe2+,其原因是 。
⑵实际生产中使用次氯酸钠的目的是 ,加入次氯酸钠后,溶液的pH
(选填“增大”“减小”“不变”),然后用试剂将溶液PH调至适当范围,即可除去铁杂质。⑶调节溶液pH宜选用的试剂是 (写序号)。
A. Ba(OH)2 B. NgCO3
C. CuO D. 稀HCl