|
下列有关除杂质(括号中为杂质)中,错误的是 | |
A. |
福尔马林(甲酸):加入足量饱和碳酸钠溶液充分振荡,蒸馏,收集馏出物 |
B. |
溴乙烷(乙醇):多次加水振荡,分液,弃水层 |
C. |
苯(苯酚):加溴水,振荡,过滤除去沉淀 |
D. |
乙酸乙酯(乙酸):加氢氧化钠溶液,充分振荡,分液,弃水层 |
|
已知某温度下,0.1 mol·L-1 NaHA的强电解质溶液中,c(H+)<c(OH-), 则下列关系一定正确的是 | |
A. |
c(Na+)=c(HA-)+2c(A2-)+c(OH-) |
B. |
c(H+)·c(OH-)=10-14 |
C. |
c(H2A)+c(HA-)+c(A2-)=0.1 mol·L-1 |
D. |
c(A2-)+c(OH-)=c(H+)+c(H2A) |
|
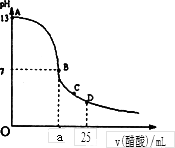
室温下, 在25 mL 0.1 mol/L NaOH溶液中逐滴加入0.2 mol/L CH3COOH溶液,曲线如下图所示,若忽略两溶液混合时的体积变化,有关粒子浓度关系比较错误的是
| |
A. |
在A、B间任一点,溶液中一定都有:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
B. |
在B点:a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+) |
C. |
在C点:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
D. |
在D点:c(CH3COO-)+c(CH3COOH)=0.1 mol/L |
|
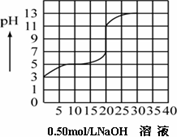
在100毫升某一元弱酸(Ka=10-3~10-7)的溶液中,以0.50 mol/L氢氧化钠溶液滴定后得滴定曲线如下图所示,下列叙述正确的是:
| |
A. |
该弱酸在滴定前的浓度是0.15 mol/L: |
B. |
该弱酸的电离常数(Ka)是10-5 |
C. |
在滴定过程,为求滴定终点,最合适的指示剂是酚酞 |
D. |
在滴定过程,为求滴定终点,最合适的指示剂是甲基橙 |
|
已知25℃时有关弱酸的电离平衡常数:则下列有关说法正确的是
| |
A. |
等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) |
B. |
a mol·L-1 HCN溶液与b mol·L-1 NaOH溶液等体积混合后,所得溶液中c(CN-)>c(Na+),则a一定大于b |
C. |
冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离度、pH均先增大后减小 |
D. |
NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
|
已知甲酸钠(HCOONa)溶液呈碱性.室温下用pH相同、体积相同的盐酸与甲酸(HCOOH)溶液分别进行如下实验,下列相关叙述正确的是 | |
A. |
分别加入等体积水稀释,盐酸中c(H+)比甲酸中c(H+)小 |
B. |
分别用等物质的量浓度的NaOH溶液中和,盐酸比甲酸消耗的碱液少 |
C. |
分别跟等质量铝粉反应,盐酸比甲酸的起始反应速率快 |
D. |
分别跟过量的锌粒反应,盐酸比甲酸产生氢气的量多 |
|
若在加入铝粉能放出H2的溶液中分别加入下列各组离子,肯定不能共存的是 | |
A. |
Fe2+、NO |
B. |
Ba2+、Mg2+、CO |
C. |
NO |
D. |
NO |
|
有多种金属组成的混合物粉末12 g与足量的稀盐酸反应,生成11.2 L(标况)H2,则该混合物可能由________构成. | |
A. |
Fe Zn Al |
B. |
Zn Mg |
C. |
Mg Al Fe |
D. |
Al Mg |