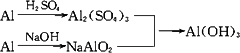|
在托盘天平右盘上放一个盛有100 mL 3 mol·L-1 NaOH溶液的烧杯,左盘上放一个盛有100 mL 3 mol·L-1盐酸的烧杯,调节天平至平衡,然后在两个烧杯中各加入等质量的铝片,反应完全后,则天平可能出现的情况是 | |
A. |
左盘下沉 |
B. |
右盘下沉 |
C. |
仍保持平衡 |
D. |
无法判断 |
|
向100 mL 2 mol·L-1的AlCl3溶液中加入一定量1 mol·L-1 NaOH溶液得到7.8 g沉淀物,则加入的NaOH溶液的体积可能是 | |
A. |
200 mL |
B. |
300 mL |
C. |
500 mL |
D. |
700 mL |
|
有镁、铝混合粉末10.2 g,将它溶于500 mL 4 mol·L-1的盐酸中,若要使沉淀的质量最大,则需加入2 mol·L-1的NaOH溶液的体积为 | |
A. |
1 000 mL |
B. |
100 mL |
C. |
1 500 mL |
D. |
2 000 mL |
|
用稀H2SO4、NaOH溶液和金属铝为原料制取Al(OH)3,甲、乙、丙三个同学制备的途径分别是: 甲:Al 乙:Al 丙: 若要得到等量的Al(OH)3,则 | |
A. |
三者消耗原料相同 |
B. |
甲消耗原料最多 |
C. |
乙消耗原料最少 |
D. |
丙消耗原料最少 |
|
已知氨水的密度为0.990 g·mL-1时,NH3的质量分数为2%,氨水的密度为0.930 g·mL-1时,NH3的质量分数为18%.溶质质量分数分别为a%和5a%的氨水按等体积混合后,混合溶液中NH3的质量分数为 | |
A. |
3a% |
B. |
6a% |
C. |
大于3a% |
D. |
小于3a% |
|
某研究性学习小组为了探索镁粉与溴水反应的机理,做了如下四组实验: ①将镁粉投入冷水中,未见任何现象; ②将镁粉放入溴水中,观察到只是开始时产生极少量的气泡,但溴水逐渐褪色; ③将镁粉放入液溴中,未观察到任何明显现象; ④向含足量镁粉的液溴中滴加几滴水,观察到溴的红棕色很快褪去. 则下列关于镁与溴水的反应机理的论述中正确的是 | |
A. |
镁粉只能直接与溴水中的溴反应 |
B. |
水是镁粉与溴发生反应的催化剂 |
C. |
产生极少量的气泡是由于镁粉与水反应得到 |
D. |
镁粉与溴水中的酸发生反应,导致平衡移动使溴水褪色 |
|
下列离子方程式书写正确的是 | |
A. |
氯气溶于水:Cl2+H2O |
B. |
氯气和烧碱反应:Cl2+OH- |
C. |
HCl气体通入AgNO3溶液中:HCl+Ag+ |
D. |
钠和水作用:Na+2H2O |