|
将 SO2少量通入Fe2(SO4)3溶液中发生反应:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+;然后再加入K2Cr2O7溶液,发生反应:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O.下列判断正确的是 | |
A. |
还原性Cr3+>Fe2+>SO2 |
B. |
氧化 |
C. |
两个反应中Fe2(SO4)3均作还原剂 |
D. |
Cr2O72-能将SO2氧化成SO42- |
|
1 mol X跟a mol Y在体积可变的密闭容器中发生如下反应:X(g)+aY(g) | |
A. |
a=1,b=1 |
B. |
a=2,b=1 |
C. |
a=2,b=2 |
D. |
a=3,b=2 |
|
在一定温度下,向a L密闭容器中加入1 mol X气体和2 mol Y气体,发生如下反应: X(g)+2Y(g) | |
A. |
容器内压强不随时间变化 |
B. |
容器内各物质的浓度不随时间变化 |
C. |
容器内X、Y、Z的浓度之比为1∶2∶2 |
D. |
单位时间消耗0.1 mol X同时生成0.2 mol Z |
|
下列各表述与示意图一致的是
| |
A. |
图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化 |
B. |
图②中曲线表示反应2SO2(g)+O2(g) |
C. |
图③表示10 mL 0.01 mol·L-1 KMnO4酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+)随时间的变化 |
D. |
图④中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g);ΔH<0使用和未使用催化剂时,反应过程中的能量变化 |
|
已知3.6 g碳在6.4 g氧气中燃烧,当两者完全消耗完时,放出X kJ热量.已知碳的燃烧热为Y kJ/mol,则1 mol碳(s)与氧气反应生成CO(g)的反应热ΔH为: | |
A. |
-(5X- |
B. |
-(10X-Y)kJ/mol |
C. |
-(X-Y)kJ/mol |
D. |
(10X-Y)kJ/mol |
|
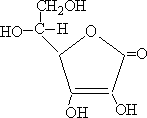
维生素C又叫L-抗坏血酸,具有酸性和较强还原性,易被氧化,其结构简式如图:下列有关维生素C的说法中不正确的是:
| |
A. |
维生素C是一种羧酸,该分子的不饱和度为3, |
B. |
向少量KMnO4溶液中滴入维生素C,可见紫色褪去 |
C. |
一定条件下,维生素C既能与乙酸反应,又可与溴水用 |
D. |
维生素C分子中含有1个手性碳原子 |
|
有两种物质的量浓度相等的溶液,把它们等体积混合有白色沉淀生成,加入过量稀HNO3后,沉淀消失并放出气体,再加入AgNO3溶液又有白色沉淀生成,这两种溶液是 | |
A. |
Na2CO3 和Ca(OH)2 |
B. |
Na2CO3 和CaCl2 |
C. |
NaOH 和CuSO4 |
D. |
Na2SO4 和Ba(NO3)2 |
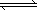 bZ(g),反应达到平衡后,测得X的转化率为50%.而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是
bZ(g),反应达到平衡后,测得X的转化率为50%.而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是 2Z(g)此反应达到平衡的标志是
2Z(g)此反应达到平衡的标志是
 2SO3(g);ΔH<0正、逆反应的平衡常数K随温度的变化
2SO3(g);ΔH<0正、逆反应的平衡常数K随温度的变化