|
分析以下几个热化学方程式,表示固态碳和气态氢气燃烧时燃烧热的是 | |
A. |
C(s)+O2(g)===CO(g) ΔH=-110.5 kJ/mol |
B. |
C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol |
C. |
2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ/mol |
D. |
H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ/mol |
|
下列各变化中属于原电池反应的是 | |
A. |
在空气中金属铝表面迅速氧化形成保护层 |
B. |
镀锌铁表面锌有划损时,也能阻止铁被氧化 |
C. |
红热的铁丝与冷水接触,表面表成蓝黑色保护层 |
D. |
锌和稀硫酸反应时,加入少量的CuSO4溶液可使反应加快 |
|
在一定温度下,向a L密闭容器中加入1 mol X气体和2 mol Y气体,发生如下反应: X(g)+2Y(g) | |
A. |
容器内压强不随时间变化 |
B. |
容器内各物质的浓度不随时间变化 |
C. |
容器内X、Y、Z的浓度之比为1∶2∶2 |
D. |
单位时间消耗0.1 mol X同时生成0.2 mol Z |
|
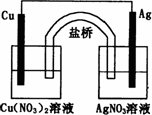
用铜片、银片、Cu(NO3) 2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池(如图).以下的叙述正确的是
①在外电路中,电流由铜电极流向银电极 ②正极反应为:Ag++e-=Ag ③实验过程中取出盐桥,原电池仍继续工作 ④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同 | |
A. |
①② |
B. |
②③ |
C. |
②④ |
D. |
③④ |
|
在10 L密闭容器中,1 mol A和3 mol B在一定条件下反应:A(气)+xB(气) | |
A. |
平衡时,物质的量比A∶B∶C=2∶11∶4 |
B. |
x 值等于4 |
C. |
B的平均反应速率为 |
D. |
A的转化率20% |
|
由二氧化碳、氢气、一氧化碳组成的混合气体在同温、同压下与氮气的密度相同.则该混合气体中二氧化碳、氢气、一氧化碳的体积比为 | |
A. |
29∶8∶13 |
B. |
22∶1∶14 |
C. |
13∶8∶13 |
D. |
26∶16∶13 |
|
下列反应中,不属于四种基本反应类型,但属于氧化还原反应的是 | |
A. |
2Na+2H2O==2NaOH+H2↑ |
B. |
CH4+2O2==CO2+2H2O |
C. |
KClO3==2KCl+3O2↑ |
D. |
CaCO3+2HCl==CaCl2+H2O+CO2↑ |