|
在100 mL 0.1 mol·L-1的CH3COOH溶液中欲使CH3COOH的电离度增大和c(H+)降低,可采用的方法是 | |
A. |
加少量1 mol·L-1的NaOH溶液 |
B. |
加少量1 mol·L-1的盐酸 |
C. |
加100 mL水 |
D. |
加热 |
|
0.1 mol·L-1的醋酸溶液加水稀释时 | |
A. |
溶液中c(H+)减小 |
B. |
溶液的酸性增强 |
C. |
c(CH3COO-)减小,电离向生成HAc的方向移动 |
D. |
平衡向电离方向移动,但c(CH3COOH)、c(H+)、c(CH3COO-)均减小 |
|
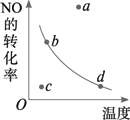
图中的曲线是表示其他条件一定时,2NO+O2
| |
A. |
a点 |
B. |
b点 |
C. |
c点 |
D. |
d点 |
|
硫的蒸气有S8、S6、S4、S2等分子,各种分子数目的多少视温度的高低而定.下列平衡随温度的升高而向右移动:3S8 | |
A. |
ρ 1=ρ2 |
B. |
ρ 1>ρ2 |
C. |
ρ 1<ρ2 |
D. |
无法计算 |
|
反应SO2+NO2 | |
A. |
平衡向正反应方向移动 |
B. |
平衡向逆反应方向移动 |
C. |
压强增大、平衡不移动 |
D. |
压强减小、平衡不移动 |
|
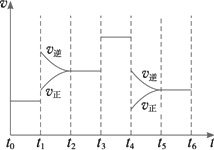
下图表示某反应N2(g)+3H2(g)
| |
A. |
t0-t1 |
B. |
t2-t3 |
C. |
t3-t4 |
D. |
t5-t6 |
|
某温度下在密闭容器中进行SO2的催化氧化,若起始浓度c(SO2)=c(O2)=6 mol·L-1,平衡时测得c(O2)=4.5 mol·L-1,则下列说法可能正确的是 | |
A. |
SO2的转化率为3 mol·L-1 |
B. |
SO3产率为50% |
C. |
平衡时的总压强与起始压强之比为3∶4 |
D. |
平衡时v(SO2)∶v(O2)∶v(SO3)=3∶2∶1 |