|
已知反应mX(g)+nY(g) | |
A. |
通入稀有气体使压强增大,平衡将正向移动 |
B. |
X的正反应速率是Y的逆反应速率的m/n倍 |
C. |
降低温度,混合气体的平均相对分子质量变小 |
D. |
增加X的物质的量,Y的转化率降低 |
|
已知:C(s)+CO2(g) | |
A. |
升高温度和减小压强 |
B. |
降低温度和减小压强 |
C. |
降低温度和增大压强 |
D. |
升高温度和增大压强 |
|
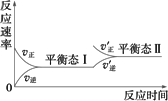
下图是在恒温密闭容器中进行的某化学反应的反应速率随时间变化的示意图.下列叙述与示意图不相不符的是
| |
A. |
反应达平衡时,正反应速率和逆反应速率相等 |
B. |
该反应达到平衡态Ⅰ后,增大反应物的浓度,平衡发生移动,达到平衡态Ⅱ |
C. |
该反应达到平衡态Ⅰ以后,减小反应物浓度,平衡发生移动,达到平衡态Ⅱ |
D. |
同一种反应物在平衡态Ⅰ和平衡态Ⅱ时浓度不相等. |
|
一定条件下,体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g) | |
A. |
以X浓度变化表示的反应速率为0.001 mol·L-1·s-1 |
B. |
将容器体积变为20 L,Z的平衡浓度变为原来的 |
C. |
若增大压强,则物质Y的转化率减小 |
D. |
若升高温度,X的体积分数增大,则该反应的ΔH>0 |
|
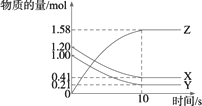
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是
| |
A. |
反应开始到10 s,用Z表示的平均反应速率为0.158 mol·(L·s)-1 |
B. |
反应开始到10 s,X的物质的量浓度减少了0.79 mol·L-1 |
C. |
反应开始到10 s时,Y的转化率为79.0% |
D. |
反应的化学方程式为:X(g)+Y(g) |
|
在一个固定容积的密闭容器中,加入m mol A,n mol B,发生反应mA(g)+nB(g) | |
A. |
a∶b∶c=m∶n∶p |
B. |
a∶b=m∶n, |
C. |
|
D. |
a= |
|
mA(s)+nB(g)
| |
A. |
n<q |
B. |
n>q |
C. |
X点,v正>v逆;Y点,v正<v逆 |
D. |
X点比Y点反应速率快
|
|
有一化学平衡mA(g)+nB(g)
| |
A. |
正反应吸热,m+n>p+q |
B. |
正反应吸热,m+n<p+q |
C. |
正反应放热,m+n>p+q |
D. |
正反应放热,m+n<p+q |
|
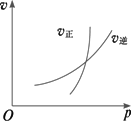
符合图中图象的反应为
| |
A. |
N2O3(g) |
B. |
3NO2(g)+H2O(l) |
C. |
4NH3(g)+5O2(g) |
D. |
CO2(g)+C(s) |
|
一定混合气体在密闭容器中发生下列反应:mA(气)+nB(气) | |
A. |
m+n>p |
B. |
A的转化率降低 |
C. |
平衡向逆反应方向移动 |
D. |
C的体积分数增加 |