|
分子式为Pt(NH3)2Cl2的配位化合物有顺铂和反铂两种同分异构体.顺铂的结构式为 | |
A. |
在水中的溶解性:顺铂>反铂 |
B. |
Pt与Ni位于同一列,则Pt位于ⅧB族 |
C. |
分子中Pt和N之间为离子键 |
D. |
分子中的N有一对孤对电子 |
|
下列说法中,正确的是 | |
A. |
冰溶化时,分子中H-O键发生断裂 |
B. |
原子晶体中,共价键的键长越短,通常熔点就越高 |
C. |
分子晶体中,共价键键能越大,该分子的熔沸点就越高 |
D. |
分子晶体中,分子间作用力越大,则分子越稳定 |
|
下表是元素周期表的一部分.表中所列的字母分别代表某一种化学元素.
下列说法正确的是 | |
A. |
沸点A2D<A2X |
B. |
CA3分子是非极性分子 |
C. |
C形成的单质中σ与π之比为1∶2 |
D. |
B、C、D形成的气态氢化物互为等电子体 |
|
对于某些离子的检验及结论一定正确的是 | |
A. |
加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO |
B. |
加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO |
C. |
加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH |
D. |
加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
|
在海水中提取溴的反应原理是5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O下列反应的原理与上述反应最相似的是 | |
A. |
2NaBr+Cl2=2NaCl+Br2 |
B. |
2FeCl3+H2S=2FeCl2+S↓+2HCl |
C. |
2H2S+SO2=3S+2H2O |
D. |
AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl |
|
下列各组中的离子,能在溶液中大量共存的是 | |
A. |
H+、Na+、CO32-、Cl- |
B. |
Ag+、Al3+、NO3-、H+ |
C. |
K+、H+、SO42-、OH- |
D. |
Ba2 +、Na+、Cl-、SO42- |
|
下列反应的离子方程式正确的是 | |
A. |
氨气通入醋酸溶液CH3COOH+NH3 |
B. |
澄清的石灰水跟盐酸反应H++OH- |
C. |
碳酸钙溶于醋酸CaCO3+2H+ |
D. |
金属钠跟水反应2Na+2H2O |
|
由一种阳离子与两种酸根离子组成的盐称为混盐.混盐CaOCl2在酸性条件下可以产生Cl2.下列关于混盐CaOCl2的有关判断正确的是 | |
A. |
该混盐中氯元素的化合价为负一价 |
B. |
该混盐的水溶液呈中性 |
C. |
该混盐与硝酸反应产生1 mol Cl2时转移1 mol电子 |
D. |
该混盐具有和漂白粉相似的化学性质 |
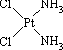 ,具有抗癌作用;反铂的结构式为
,具有抗癌作用;反铂的结构式为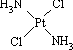 ,无抗癌作用.下列说法正确的是
,无抗癌作用.下列说法正确的是
 CH3COONH4
CH3COONH4 H2O
H2O Ca2++H2O+CO2↑
Ca2++H2O+CO2↑ 2Na++2OH-+H2↑
2Na++2OH-+H2↑