|
如图,A池用石墨电极电解NaOH溶液,B池精炼粗铜,一段时间后停止通电,A池中D极产生具有氧化性的气体在标准状况下为2.24 L.下列说法正确的是
| |
A. |
A池为电解池,B池为原电池 |
B. |
D、E两极都发生氧化反应 |
C. |
F极应为粗铜板材料 |
D. |
B池中E极质量增加12.8 g |
|
如下图所示,在一U型管中装入含有紫色石蕊的Na2SO4试液,通直流电,一段时间后U型管内会形成一个倒立的三色“彩虹”,从左到右颜色的次序是
| |
A. |
蓝、紫、红 |
B. |
红、蓝、紫 |
C. |
红、紫、蓝 |
D. |
紫、红、蓝 |
|
钠硫电池是一种高能电池,它是以熔融的钠硫为两极,以可导电的固体作电解质,反应方程式为:2Na+xS | |
A. |
放电时钠作负极,硫作正极 |
B. |
放电时钠极发生还原反应 |
C. |
充电时钠极与外电源的正极相连,硫与外电源的负极相连 |
D. |
充电时,阴极发生的反应为:Sx2--2e-=xS |
|
有Mg、Na、Zn、Ag四种金属,若两两混合后,取混合物13 g与足量的稀硫酸反应,产生H2的体积在标准状况下为11.2 L,则此混合物的组合方式最多有 | |
A. |
2种 |
B. |
3种 |
C. |
4种 |
D. |
5种 |
|
能正确表示下列反应的离子方程式是 | |
A. |
Ba(OH)2与稀H2SO4反应 Ba2++OH-+H++SO42- |
B. |
氢氧化镁与盐酸的反应 OH-+H+=H2O |
C. |
C12与NaOH溶液反应 Cl2+2OH- |
D. |
碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2↑ |
|
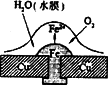
铜板上铁铆钉处的吸氧腐蚀原理如图所示,下列有关说法中,不正确的是
| |
A. |
负极电极反应式为:Fe-3e-=Fe3+ |
B. |
此过程中还涉及到反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3 |
C. |
此过程中铜并不被腐蚀 |
D. |
此过程中电子从Fe移向Cu |