|
可逆反应2NO2 ①单位时间内生成n mo1 O2的同时生成2nmol NO2 ②单位时间内生成nmol O2的同时生成2nmol NO ③混合气体的颜色不再改变 ④混合气体的密度不再改变的状态 ⑤混合气体的平均相对分子质量不再改变的状态 | |
| [ ] | |
A. |
①③⑤ |
B. |
②④⑤ |
C. |
①③④ |
D. |
①②③④⑤ |
|
下列有关热化学方程式的叙述正确的是 | |
| [ ] | |
A. |
已知2H2(g)+O2(g) |
B. |
含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则表示该反应中和热的化学方程式为:NaOH(aq)+HCl(aq) |
C. |
已知C(石墨,s) |
D. |
已知2C(s)+2O2(g) |
|
某无色透明的溶液中加入铝粉能放出氢气,此溶液中一定能大量共存的离子组是 | |
| [ ] | |
A. |
H+、Cu2+、Cl-、SO42- |
B. |
HCO3-、NO3-、SO42-、Na+ |
C. |
Cl-、SO42-、K+、Na+ |
D. |
Fe3+、SO42-、Cl-、Al[(OH)4]- |
|
已知短周期元素的离子aA2+、bB+、cC2-、dD-具有相同的电子层结构.则下列叙述正确的是 | |
| [ ] | |
A. |
原子半径A>B>C>D |
B. |
离子半径C2->D->B+>A2+ |
C. |
原子序数d>c>b>a |
D. |
原子的失电子能力A>B>D>C |
|
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
| |
| [ ] | |
A. |
常压下五种元素的单质中,Z单质的沸点最高 |
B. |
Y、Z的阴离子电子层结构都与R原子相同 |
C. |
酸性H3WO4>HXO3 |
D. |
Y元素的非金属性比W元素的非金属性强 |
|
从松树中分离得到的松柏醇,其结构简式为, | |
| [ ] | |
A. |
1 mol,2 mol |
B. |
4 mol,2 mol |
C. |
4 mol,4 mol |
D. |
4 mol,1 mol |
|
一氧化碳、烯烃和氢气在催化剂作用下发生烯烃的醛化反应,又叫羰基的合成.如由乙烯可制丙醛:CH2=CH2+CO→CH3CH2CHO,由丁烯进行醛化反应也可得到醛,在它的同分异构体中属于醛的共有 | |
| [ ] | |
A. |
2种 |
B. |
3种 |
C. |
4种 |
D. |
5种 |
|
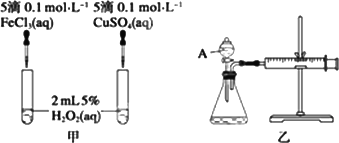
为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲、乙两位同学分别设计了如图甲、乙所示的实验.下列叙述中正确的是
| |
| [ ] | |
A. |
图甲所示实验无法直接比较反应速率的大小 |
B. |
若图甲所示实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好. |
C. |
用图乙所示装置测定反应速率时,可测定反应产生的气体体积及反应时间 |
D. |
为检查图乙所示装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离后松开活塞,若一段时间后观察活塞不能回到原位,说明气密性良好. |