|
居里夫人发现了放射性元素镭 (Ra),因而获得诺贝尔化学奖,已知镭原子核内有88个质子,与Ca处于同一主族.下列说法不正确的是 | |
| [ ] | |
A. |
镭位于周期表中第七周期 IIA族 |
B. |
镭的硫酸盐难溶于水 |
C. |
镭的碳酸盐可溶于水 |
D. |
镭的氢氧化物为强碱 |
|
A、B为短周期元素,二者可以组合成多种中学生所熟知的化合物.在这些化合物中,A与B的原子个数比为A∶B=1∶2.已知A的原子序数为n,B的原子序数是①n+2、②n+3、③n+4、④n+5、⑤n+8、⑥n-5、⑦n-6、⑧n-8中的几种,其中不符合题目要求的是 | |
| [ ] | |
A. |
①④ |
B. |
②⑧ |
C. |
③⑤ |
D. |
⑥⑦ |
|
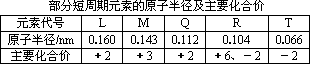
A、B都是短周期元素,原子半径B>A,它们可形成化合物AB2,由此可以得出的正确判断是 | |
| [ ] | |
A. |
原子序数:A﹥B |
B. |
A和B可能在同一主族 |
C. |
A可能在第2周期ⅣA族 |
D. |
A肯定是金属元素 |
|
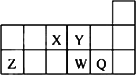
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是
| |
| [ ] | |
A. |
元素X与元素Z的最高正化合价之和的数值等于8 |
B. |
原子半径的大小顺序为:rX>rY>rZ>rW>rQ |
C. |
离子Y2-和Z3+的核外电子数和电子层数都不相同 |
D. |
元素W的最高价氧化物对应的水化物的酸性比Q的强 |
|
甲、乙两种非金属:①甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强;②甲比乙更容易与氢气化合;③甲单质能与乙阴离子发生氧化还原反应;④与金属反应时,甲原子得电子数目比乙的多;⑤甲的单质熔沸点比乙的低.能说明甲比乙的非金属性强的是 | |
| [ ] | |
A. |
①②③④ |
B. |
①②③④⑤ |
C. |
①②③ |
D. |
②③④⑤ |
|
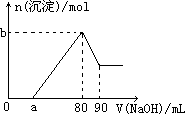
把一块镁铝合金投入到1 mol/L盐酸中,待合金完全溶解后,再往溶液里加入1 mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化如图所示.
下列说法中错误的是 | |
| [ ] | |
A. |
盐酸的体积为80 mL |
B. |
a的取值范围为0<a<50 |
C. |
n(Mg2+)<0.025 mol |
D. |
当a值为30时,b值为0.01 |
|
下列离子方程式中,正确的是 | |
| [ ] | |
A. |
铁与氯化铁溶液反应:Fe+Fe3+ |
B. |
大理石与稀盐酸反应:CO |
C. |
铜与稀硝酸反应:Cu+H++NO |
D. |
氯气与氢氧化钠溶液反应:Cl2+2OH- |