|
下列溶液中各微粒的浓度关系不正确的是 | |
| [ ] | |
A. |
0.1 mol/L CH3COOH溶液中:c(CH3COO-)+c(CH3COOH)=0.1 mol/L |
B. |
NaHCO3溶液中:c(OH-)=c(H+)+c(H2CO3)-c(CO |
C. |
CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
D. |
Na2S 溶液中:2c(Na+)=c(S2-)+c(HS-)+c(H2S) |
|
下列有关热化学方程式的叙述中,正确的是 | |
| [ ] | |
A. |
含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则表示该反应中和热的热化学方程式为NaOH(aq)+HCl(aq) |
B. |
已知C(石墨,s) |
C. |
已知2H2(g)+O2(g) |
D. |
已知C(s)+O2(g) |
|
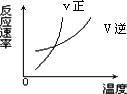
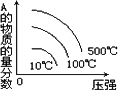
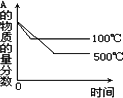
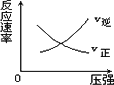
对于可逆反应X(g)+Y(g) | |
| [ ] | |
A. |
a mol X+a mol Y |
B. |
2a mol Z |
C. |
a mol X+a mol Z |
D. |
a mol Y+a mol Z |
|
2.0 mol PCl3和 1.0 mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g) | |
| [ ] | |
A. |
0.40 mol |
B. |
0.20 mol |
C. |
小于0.20 mol |
D. |
大于0.20 mol,小于0.40 mol |
|
室温时 ,将浓度和体积分别为c1、V1的NaOH溶液和c2、V2的CH3COOH溶液相混合,下列关于该混合溶液的叙述错误的是 | |
| [ ] | |
A. |
若 pH>7,则一定是c1V1=c2V2 |
B. |
在任何情况下都是 c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
C. |
当 pH=7时,若V1=V2,一定是c2>c1 |
D. |
若 V1=V2,c1=c2,则c(CH3COO-)+c(CH3COOH)=c(Na+) |
|
在25℃时,某溶液中由水电离出的c(H+)=1.0×10-12 mol/L,则该溶液中一定能够大量共存的离子组是 | |
| [ ] | |
A. |
K+、Fe2+、SO |
B. |
K+、Na+、HCO |
C. |
Na+、Ag+、I-、NO |
D. |
Ba2+、Na+、Cl-、NO |
|
25℃时,将稀氨水逐滴加入到稀硫酸中,当溶液的pH=7时,下列关系正确的是 | |
| [ ] | |
A. |
c (NH |
B. |
2c(NH |
C. |
c (NH |
D. |
c (OH-)+c(SO |
|
设NA表示阿伏加德罗常数的数值,下列叙述中正确的是 | |
| [ ] | |
A. |
28 g以任意比组成的CO与N2混合气体中含有原子数为2NA |
B. |
标准状况下,22.4 L H2O含有的分子数为NA |
C. |
在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移4NA个电子 |
D. |
1 L 1 mol/L的盐酸中有NA个HCl分子 |
|
在溶液中能大量共存 ,加入OH-有沉淀产生,加入H+有气体放出的是 | |
| [ ] | |
A. |
Na+ 、Cu2+、Cl-、SO |
B. |
Fe3+ 、K+、SO |
C. |
H+ 、Al3+、OH-、NO |
D. |
Na+ 、Ca2+、Cl-、HCO |