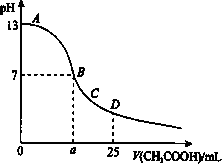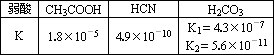|
下列离子方程式表达正确的是 | |
| [ ] | |
A. |
SO2通入溴水中溴水褪色:SO2+2H2O+Br2=2H++SO |
B. |
漂白粉溶液在空气中失效 :ClO-+CO2+H2O=HClO+HCO |
C. |
NaHSO4 溶液和Ba(OH)2溶液充分反应后溶液呈中性:Ba2++2OH-+2H++SO |
D. |
Fe(OH)3 溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O |
|
NA 表示阿伏加德罗常数的值,下列说法正确的是 | |
| [ ] | |
A. |
0.012 千克石墨晶体中含共用电子对数目为2NA |
B. |
电解精炼铜时,若阴极得到电子数为 2NA个,则阳极溶解的铜的质量为小于64 g |
C. |
常温常压下 ,32 g O2和O3的混合气体所含原子数为NA |
D. |
20℃ 、1.01×105 Pa时,2.24 L C2H4和CO的混合气体,含气体分子数为0.1NA |
|
将 17.9 g Al、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生3.36 L气体(标准状况).另取等质量的该合金溶于过量的稀硝酸中,生成6.72 L NO(标准状况),向反应后的溶液中加入足量的NaOH溶液,得到沉淀的质量为 | |
| [ ] | |
A. |
33.2 g |
B. |
25.4 g |
C. |
22.4 g |
D. |
19.6 g |
|
在 25 mL 0.1 mol/L NaOH溶液中逐滴加入0.2 mol/L CH3COOH溶液,曲线如图所示,下列有关离子浓度关系的比较,正确的是
| |
| [ ] | |
A. |
在 A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
B. |
在 B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+) |
C. |
在 C点:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
D. |
在 D点:c(CH3COO-)+c(CH3COOH)>2c(Na+) |
|
有Fe2+、NO | |
| [ ] | |
A. |
氧化剂与还原剂的物质的量之比为1∶8 |
B. |
该过程说明Fe(NO3)2溶液不宜加酸酸化 |
C. |
若有1 mol NO |
D. |
若把该反应设计为原电池,则负极反应为Fe2+-e- |
|
甲、乙、丙是三种不含相同离子的可溶性强电解质.它们所含离子如下表所示:
取等质量的三种化合物配制相同体积的溶液,其溶质物质的量浓度:c(甲)>c(乙)>c(丙),则乙物质可能是 ①MgSO4 ②NaOH ③(NH4)2SO4 ④Mg(NO3)2 ⑤NH4NO3 | |
| [ ] | |
A. |
①② |
B. |
③④ |
C. |
③⑤ |
D. |
①⑤ |
|
某溶液中可能含有Na+、NH | |
| [ ] | |
A. |
Na+ |
B. |
SO |
C. |
Ba2+ |
D. |
NH |
|
25℃时,弱酸的电离平衡常数如右表,下列说法正确的是
| |
| [ ] | |
A. |
等物质的量浓度溶液pH关系:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) |
B. |
amol/L HCN与bmol/L NaOH溶液等体积混合后所得溶液中c(Na+)>c(CN-),则a一定小于b |
C. |
往冰醋酸中逐滴加水,溶液导电能力先增大,后减小 |
D. |
NaHCO3和Na2CO3的混合液中:c(Na+)+c(H+)=c(OH-)+c(HCO |
|
25℃时,浓度均为0.1 moI·L-l的HA溶液和BOH溶液,pH分别是l和11.下列说法正确的是 | |
| [ ] | |
A. |
BOH溶于水,其电离方程式是BOH=B++OH- |
B. |
若一定量的上述两溶液混合后pH=7,则c(A-)=c(B+) |
C. |
在0.1 mol·L-l BA溶液中,c(B+)>c(A-)>c(OH-)>c(H+) |
D. |
若将0.1 mol·L-l BOH溶液稀释至0.001 mol·L-1,则溶液的pH=9 |
|
氧化还原反应实际上包含氧化和还原两个过程:①向氯酸钠的酸性水溶液中通入二氧化硫,该反应中氧化过程的反应式为:SO2+2H2O-2e-→SO | |
| [ ] | |
A. |
NaClO |
B. |
HClO |
C. |
ClO2 |
D. |
NaClO4 |