|
下列离子方程式的书写不正确的是 | |
| [ ] | |
A. |
氢氧化钡溶液与衡硫酸反应:Ba2++SO42-+H++OH- |
B. |
Ca(ClO)2溶液中通入过量CO2:ClO-+H2O+CO2 |
C. |
铜溶于稀硝酸:3Cu+8H++2NO3- |
D. |
将AlCl3溶液滴入氨水中:3NH3·H2O+Al3+ |
|
用NA表示阿伏加德罗常数的值,下列说法正确的是 | |
| [ ] | |
A. |
标准状况下,5.6 L NO和5.6 L O2混合后的分子总数为0.5NA |
B. |
1 mol Na2O2固体中含离子总数为4NA |
C. |
7.1 g Cl2与足量NaOH溶液反应转移的电子数为0.2NA |
D. |
在标准状况下,22.4 L CH4与18 g H2O所含有的电子数均为10NA |
|
下列离子反应方程式正确的是 | |
| [ ] | |
A. |
用两个铜电极电解食盐水:2Cl-+2H2O |
B. |
腐蚀法制作印刷线路板:Fe3++Cu |
C. |
以铜作电极电解硫酸铜溶液:2Cu2++2H2O |
D. |
AlCl3 溶液呈酸性的原因:Al3++3H2O |
|
将氢气、甲烷、乙醇等物质在氧气中燃烧时的化学能直接转化为电能的装置叫燃料电池.燃料电池的基本组成为电极、电解质、燃料和氧化剂.此种电池能量利用率可高达80%(一般柴油发电机只有40%左右),产物污染也少.下列有关燃料电池的说法错误的是 | |
| [ ] | |
A. |
上述燃料电池的负极反应材料是氢气、甲烷、乙醇等物质 |
B. |
氢氧燃料电池常用于航天飞行器,原因之一是该电池的产物为水,经过处理之后可供宇航员使用 |
C. |
乙醇燃料电池的电解质常用KOH,该电池的负极反应为C2H5OH-12e-=2CO2↑+3H2O |
D. |
甲烷燃料电池的正极反应为O2+2H2O+4e-=4OH- |
|
a、b、c、d是四种短周期元素.a、b、d同周期,c、d同主族.a的原子结构示意图为 | |
| [ ] | |
A. |
原子半径:a>c>d>b |
B. |
电负性a>b>d>c |
C. |
原子序数:d>a>c>b |
D. |
最高价含氧酸的酸性c>d>a |
|
下图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是
①X的气态氢化物与Y的最高价氧化物对应的水化物能发生反应生成盐; ②Y、Z的气态氢化物水溶液的酸性Y<Z; ③Z的单质常温下是液体,可与铁粉反应; ④Z的原子序数比Y大19; ⑤Z所在的周期中含有32种元素. | |
| [ ] | |
A. |
①②③④ |
B. |
①②③④⑤ |
C. |
只有③ |
D. |
只有①④ |
|
下列说法中正确的是 | |
| [ ] | |
A. |
NO2、SO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8电子稳定结构; |
B. |
P4和CH4都是正四面体分子且键角都为109° |
C. |
NaCl晶体中与每个Na+距离相等且最近的Na+共有12个; |
D. |
单质的晶体中一定不存在的微粒是阳离子 |
|
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是 | |
| [ ] | |
A. |
X与Y形成化合物时,X显负价,Y显正价 |
B. |
第一电离能Y一定小于X |
C. |
最高价含氧酸的酸性:X对应的酸性强于Y对应的酸性 |
D. |
气态氢化物的稳定性:HmY小于HmX |
|
氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水发生反应,有关叙述正确的是 | |
| [ ] | |
A. |
氯化硼液态时能导电而固态时不导电 |
B. |
硼原子以sp杂化 |
C. |
氯化硼遇水蒸气会产生白雾 |
D. |
氯化硼分子属极性分子 |
|
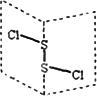
氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如下图所示.常温下S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体.
下列说法错误的是 | |
| [ ] | |
A. |
S2Cl2的结构式为Cl-S-S-Cl |
B. |
S2Cl2为含有极性键和非极性键的非极性分子 |
C. |
S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2 |
D. |
S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl |
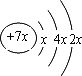 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为