|
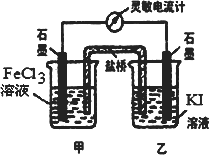
控制合适的条件,将反应2Fe3++2I-
| |
| [ ] | |
A. |
反应开始时,乙中石墨电极上发生氧化反应 |
B. |
反应开始时,甲中石墨电极上Fe3+被还原 |
C. |
电流计读数为零时,反应达到化学平衡状态 |
D. |
电流计读数为零后,在甲中加入FeCl2固体,乙中石墨电极为负极 |
|
下列离子方程式正确的是 | |
| [ ] | |
A. |
用铂电极电解氯化镁溶液:2Cl-+2H2O |
B. |
Fe(OH) 3溶于氢碘酸:Fe(OH)3+3H+ |
C. |
稀硝酸和过量的铁屑反应:3Fe+8H++2NO |
D. |
含等物质的量的NaHCO3和Ba(OH)2溶液混合: HCO |
|
下列各组中的离子,能在溶液中大量共存的有 | |
| [ ] | |
A. |
Na+、H+、CO32-、Cl- |
B. |
Na+、Ba2+、Cl-、SO42- |
C. |
K+、H+、SO42-、OH- |
D. |
Ag+、Al3+、NO3-、H+ |
|
将Mg、Cu组成的2.64 g混合物投入适量稀硝酸中,固体完全溶解时收集到的还原产物NO气体0.896 L(标准状况),向反应后溶液中加入2 mol/L NaOH溶液60 mL时金属离子恰好沉淀完全.则形成沉淀质量及硝酸物质的量分别为 | |
| [ ] | |
A. |
4.32 g 0.02 mol |
B. |
4.68 g 0.16 mol |
C. |
5.36 g 0.18 mol |
D. |
6.38 g 0.2 mol |
|
下列离子方程式正确的是 | |
| [ ] | |
A. |
FeCl3溶液中滴加过量Na2S溶液:2Fe3++S2-═2Fe2++S↓ |
B. |
将Na2O2固体投入H218O中:2Na2O2+2H218O=4Na++4OH-+18O2↑ |
C. |
向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液,恰好使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-=Al(OH)3↓+NH3·H2O+2BaSO4↓ |
D. |
少量CO2通入苯酚钠溶液中:2C6H5O-+CO2+H2O=2C6H5OH+CO32- |
|
标准状况下,将a L H2和Cl2的混合气体点燃,充分反应后,将混合气体通入含b mol NaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl-、ClO-、ClO3-,则原混合气体中H2的物质的量为 | |
| [ ] | |
A. |
a/2mol |
B. |
(a/22.4-b)mol |
C. |
(a/22.4-b/2)mol |
D. |
b/2mol |
|
下列各组溶液中,可能大量共存的离子有 | |
| [ ] | |
A. |
含有大量Ba2+的溶液中:HCO3-、Ag+、Fe3+、Cl- |
B. |
滴加甲基橙试液后呈红色的溶液中:Na+、CO32-、K+、AlO2- |
C. |
由水电离的c(OH-)=10-14 mol·L-1的溶液中:CH3COO-、C6H5O-、Na+、K+ |
D. |
加入铝粉后产生氢气的溶液中:NH4+、Na+、NO3-、Cl- |
|
pH=3的盐酸和pH=11的氨水等体积混合,溶液中离子浓度关系正确的是 | |
| [ ] | |
A. |
c(NH |
B. |
c(NH |
C. |
c(Cl-)>c(NH |
D. |
c(Cl-)>c(NH |
|
向质量分数为2a%,体积为10 mL,物质的量浓度为c1 mol·L-1的稀H2SO4中加入VmL的水,使之质量分数为a%,此时物质的量浓度为c2 mol·L-1,则下列关系正确的是 | |
| [ ] | |
A. |
V >10 mL 2c2=c1 |
B. |
V <10 mL 2c2>c1 |
C. |
V >10 mL 2c2<c1 |
D. |
V >10 mL 2c2>c1 |