|
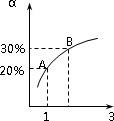
某温度下 ,对于反应N2(g)+3H2(g)N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是:\
| |
| [ ] | |
A. |
将1.0 mol氮气、3.0 mol氢气,置于1L密闭容器中发生反应,放出的热量为92.4 kJ. |
B. |
平衡状态由A变到B时,平衡常数K(A)<K(B). |
C. |
上述反应在达到平衡后,增大压强,H2的转化率提高. |
D. |
升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小. |
|
下列说法或表示方法正确的是 | |
| [ ] | |
A. |
若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
B. |
由“C(石墨)=C(金刚石) ΔH=1.9 kJ/mol”可知,金刚石比石墨稳定 |
C. |
在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=285.8 kJ/mol |
D. |
在稀溶液中:H++OH-=H2O ΔH=-57.3 kJ/mol,若将含1 mol CH3COOH与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJ |
| |||||||||||||||||||||||||||||||||||||||||||||
|
一定温度下,可逆反应2NO2 ①单位时间内生成n mol O2,同时生成2n mol NO2 ②单位时间内生成n mol O2,同时生成2n mol NO ③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1 ④混合气体的压强不再改变 ⑤混合气体的颜色不再改变 ⑥混合气体的平均相对分子质量不再改变 | |
| [ ] | |
A. |
①④⑤⑥ |
B. |
①②③⑤ |
C. |
②③④⑥ |
D. |
以上全部 |
|
用过量铁片与稀盐酸反应,为加快其反应速率而使生成氢气量不变,下列措施中可行的是 ①以铁屑代替铁片 ②用过量锌片代替铁片 ③在稀盐酸中加入少量CuSO4溶液 ④在稀盐酸中加入CH3COONa固体 ⑤在稀盐酸中加入等物质的量浓度的硫酸溶液 ⑥在稀盐酸中加入硫酸钾溶液 ⑦微热(不考虑HCl的挥发) ⑧在稀盐酸中加入Na2CO3固体 | |
| [ ] | |
A. |
除④外 |
B. |
除④⑤⑥⑧外 |
C. |
除④⑥外 |
D. |
全部都可行 |
|
胡椒酚是植物挥发油中的一种成分.关于胡椒酚的下列说法: ①该化合物属于芳香烃; ②分子中至少有7个碳原子处于同一平面; ③它的部分同分异构体能发生银镜反应; ④1 mol该化合物最多可与2 mol Br2发生反应. 其中正确的是
胡椒酚 | |
| [ ] | |
A. |
①③ |
B. |
①②④ |
C. |
②③ |
D. |
②③④ |
|
某羧酸衍生物A,其分子式为C6H12O2,实验表明A和氢氧化钠溶液共热生成B和C,B和盐酸反应生成有机物D,C在铜催化和加热条件下氧化为E,其中D、E都不能发生银镜反应.由此判断A可能的结构有 | |
| [ ] | |
A. |
6种 |
B. |
4种 |
C. |
3种 |
D. |
2种 |
|
一定质量的某有机物和足量钠反应,可得到气体VA L,等质量的该有机物如果与足量的纯碱反应,可得到气体VB L,若同温同压下VA>VB,则该有机物可能是 | |
| [ ] | |
A. |
HO(CH2)2COOH |
B. |
HO-(CH2)2-CHO |
C. |
HOOC-COOH |
D. |
CH3COOH |
|
将20 mL 0.4 mol·L-1硝酸铵溶液跟50 mL 0.1 mol·L-1氢氧化钡溶液混合,则混合溶液中各离子浓度的大小顺序是 | |
| [ ] | |
A. |
c( |
B. |
c( |
C. |
c(Ba2+)>c( |
D. |
c( |
 CuCl2+H2O,FeO+2HCl
CuCl2+H2O,FeO+2HCl FeCl2+H2O.已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀.
FeCl2+H2O.已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀. 2NO+O2在体积固定的密闭容器中反应,达到平衡状态的标志是
2NO+O2在体积固定的密闭容器中反应,达到平衡状态的标志是