|
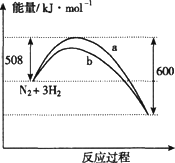
下图是198 K时N2与H2反应生成NH3的过程中能量变化的曲线图.下列叙述正确
| |
| [ ] | |
A. |
该反应的热化学方程式为: N2(g)+3H2(g) |
B. |
a曲线是加入催化剂时的能量变化曲线 |
C. |
加入催化剂,该化学反应的反应热改变 |
D. |
在温度体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ则184>Q2>2Q1 |
|
对下列各组离子的叙述不正确的是 | |
| [ ] | |
A. |
H+、 |
B. |
Mg2+、 |
C. |
Fe3+、K+、 |
D. |
Na+、 |
|
下列离子方程式正确的是 | |
| [ ] | |
A. |
向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O |
B. |
向溴化亚铁溶液通入过量氯气:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 |
C. |
向含1mol[NH4Al(SO4)2]的稀溶液中逐滴加入含2 mol Ba(OH)2的稀溶液: NH |
D. |
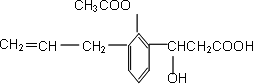
尼泊金酸(
|
|
反应aM(g)+bN(g)
| |
| [ ] | |
A. |
同温同压同Z时,加入催化剂,平衡时Q的体积分数增加 |
B. |
同温同压时,增加Z,平衡时Q的体积分数增加. |
C. |
同温同Z时,增加压强,平衡时Q的体积分数增加 |
D. |
同压同Z时,升高温度,平衡时Q的体积分数增加 |
|
在密闭容器中,aA(气) | |
| [ ] | |
A. |
平衡向逆反应方向移动了; |
B. |
物质A的转化率减少了; |
C. |
物质B的质量分数增加了; |
D. |
a>b; |
|
在密闭容器中进行下列反应:M(气)+N(气)
| |
| [ ] | |
A. |
正反应放热,L是气体 |
B. |
正反应吸热,L是固体 |
C. |
正反应吸热,L是气体 |
D. |
正反应放热,L是固体或液体 |
|
甲醇燃料电池可用于笔记本电脑等,它一极通入氧气,另一极通入甲醇;电解质能传导H+.电池工作时,2CH3OH+3O2 | |
| [ ] | |
A. |
通甲醇一极为正极. |
B. |
正极电极反应式3O2+12H++12e-=6H2O |
C. |
电池工作时电子从氧气一极流向甲醇一极. |
D. |
当转移24 mol e-时,消耗的甲醇2 mol. |
|
铅蓄电池的工作原理为Pb+PbO2+2H2SO4
| |
| [ ] | |
A. |
K闭合时,d电极反应式:PbSO4+2H2O-2e- |
B. |
当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2 mol |
C. |
K闭合时,Ⅱ中SO42-向c电极迁移 |
D. |
K闭合一段时间后,Ⅱ可单独作为原电池,d电极为正极 |

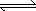 cP(g)+dQ(g)达到平衡时.M的体积分数y(M)与反应条件的关系如下图所示.其中:Z表示反应开始时N的物质的量与M的物质的量之比.下列说法正确的是
cP(g)+dQ(g)达到平衡时.M的体积分数y(M)与反应条件的关系如下图所示.其中:Z表示反应开始时N的物质的量与M的物质的量之比.下列说法正确的是
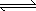 bB(气)达平衡后,保持温度不变,将容器体积增加1倍,当达到新平衡时,B的浓度是原来的60%,下列说法正确的是:
bB(气)达平衡后,保持温度不变,将容器体积增加1倍,当达到新平衡时,B的浓度是原来的60%,下列说法正确的是: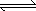 R(气)+2L(?)此反应符合下面图象,下列叙述正确的是
R(气)+2L(?)此反应符合下面图象,下列叙述正确的是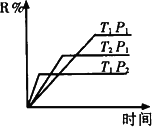
 2CO2+4H2O,下列说法正确的是
2CO2+4H2O,下列说法正确的是 2PbSO4+2H2O,研读下图,下列判断不正确的是
2PbSO4+2H2O,研读下图,下列判断不正确的是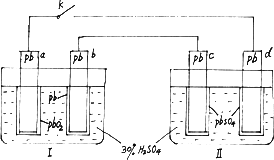
 PbO2+4H++SO42-
PbO2+4H++SO42-