|
元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构.下列推测不正确的是 | |
| [ ] | |
A. |
同周期元素中X的金属性最强 |
B. |
原子半径X>Y,离子半径X+>Z2- |
C. |
同族元素中Z的氢化物稳定性最高 |
D. |
同周期元素中Y的最高价含氧酸的酸性最强 |
|
A、B、C、D、E五种元素同周期从左向右按原子序数递增(原子序数为5个连续的自然数)的顺序排列如下:
下列说法中正确的是 | |
| [ ] | |
A. |
E元素的最高化合价为+7时,D元素的负化合价可为-2价 |
B. |
A(OH)n为强碱时,B(OH)m也一定为强碱 |
C. |
HnDOm为强酸时,E的非金属性一定很强 |
D. |
HnCOm为强酸时,E的单质可能有强还原性 |
|
元素X、Y和Z可结合形成化合物XYZ3;X、Y和Z的原子序数之和为26;Y和Z在同一周期.下列有关推测正确的是 | |
| [ ] | |
A. |
XYZ3是一种可溶于水的酸,且X与Y可形成共价化合物XY |
B. |
XYZ3是一种微溶于水的盐,且X与Z可形成离子化合物XZ |
C. |
XYZ3是一种易溶于水的盐,且Y与Z可形成离子化合物YZ |
D. |
XYZ3是一种离子化合物,且Y与Z可形成离子化合物YZ2 |
|
如图为元素周期表前四周期的一部分,
下列有关R、W、X、Y、Z,5种元素的叙述中,正确的是 | |
| [ ] | |
A. |
常压下5种元素的单质中Z单质的沸点最高 |
B. |
Y、Z的阴离子电子层结构都与R原子的相同 |
C. |
W的氢化物的还原性比Y的氢化物的还原性弱 |
D. |
Y元素的非金属性比W元素的非金属性强 |
|
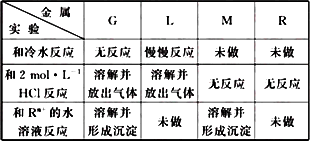
对四种金属G、L、M、R进行如下实验:
根据表中所给实验结果,判断这四种金属活动性由强到弱的次序正确的是 | |
| [ ] | |
A. |
L、G、R、M |
B. |
G、L、M、R |
C. |
L、G、M、R |
D. |
L、R、G、M |
|
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13.X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍.下列说法正确的是 | |
| [ ] | |
A. |
X的氢化物溶于水显酸性 |
B. |
Y的金属性小于Na的金属性 |
C. |
Z的氢化物的水溶液在空气中存放不易变质 |
D. |
X和Z的最高价氧化物对应的水化物都是弱酸 |
|
有a、b、c、d四种元素,a、b为同周期元素,c、d为同主族元素.已知a的阳离子和d的阴离子具有相同的电子层结构.b的阴离子和c的阴离子电子层结构相同.且c离子的电荷数大于b离子.则下列说法正确的是 ①原子序数d<b<c<a ②原子序数d<a<c<b ③原子序数d<a<b<c ④离子半径b>c>d>a ⑤离子半径b>c>a>d ⑥离子半径c>b>d>a | |
| [ ] | |
A. |
③④ |
B. |
②⑥ |
C. |
①⑤ |
D. |
②④ |
|
下列排列顺序正确的是 ①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O ③酸性:H3PO4>H2SO4>HClO4 ④结合质子能力:OH->CH3COO->Cl- | |
| [ ] | |
A. |
①③ |
B. |
②④ |
C. |
①④ |
D. |
②③ |
|
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是 | |
| [ ] | |
A. |
原子半径:r(A)>r(B)>r(D)>r(C) |
B. |
原子序数:d>c>b>a |
C. |
离子半径:r(C3-)>r(D-)>r(B+)>r(A2+) |
D. |
单质的还原性:A>B>D>C |