|
下列除去杂质的方法正确的是 ①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离; ②除去乙酸乙酯中少量的乙酸:用饱和碳酸氢钠溶液洗涤,分液、干燥、蒸馏; ③除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶; ④除去乙醇中少量的乙酸:加足量生石灰,蒸馏. | |
| [ ] | |
A. |
①② |
B. |
②④ |
C. |
③④ |
D. |
②③ |
|
某工厂的废渣中混有少量的锌粉和氧化铜(其他成分不跟酸反应),跟大量废盐酸接触形成污水,产生公害.若向污水中撒入铁粉且反应后铁粉有剩余,此时污水中一定含有的金属离子是 | |
| [ ] | |
A. |
Fe2+、Cu2+ |
B. |
Cu2+ 、H+ |
C. |
Zn2+、Fe2+ |
D. |
Zn2+、H+ |
|
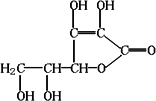
维生素C是一种水溶性维生素(其水溶液呈酸性)化学式为C6H8O6,结构如下图所示.人体缺乏这种维生素C易得坏血症,所以维生素C又称抗坏血酸.维生素C易被空气中的氧气氧化.在新鲜的水果、蔬菜、乳制品中都含维生素C,如新鲜的橙汁中维生素C的含量在500 mg/L左右.下列关于维生素C的叙述错误的是
| |
| [ ] | |
A. |
维生素C能使溴水褪色 |
B. |
维生素C可作食品添加剂 |
C. |
维生素C可发生水解反应 |
D. |
维生素C不能发生氧化反应 |
|
有一混合溶液,其中只含有Fe2+、Cl-、Br-、I-(忽略水的电离),其中Cl-、Br-、I-的个数比为2∶3∶4,向该溶液中通入氯气,使溶液中Cl-和Br-的个数比为3∶1,则通入氯气的物质的量与溶液中剩余的Fe2+的物质的量之比为(还原性I->Fe2+>Br->Cl-) | |
| [ ] | |
A. |
7∶1 |
B. |
7∶2 |
C. |
7∶3 |
D. |
7∶4 |
|
“甲型H1N1”流感疫情已构成“具有国际影响的公共卫生紧急事态”.已知扎那米韦是流感病毒神经氨酸酶抑制剂,其对流感病毒的抑制是以慢结合的方式进行的,具有高度特异性,其分子结构如图所示.下列说法正确的是
| |
| [ ] | |
A. |
该物质的分子式为C12H19N4O7 |
B. |
1 mol该物质与NaOH溶液反应,可以消耗4 mol NaOH |
C. |
在一定条件下,该物质可以发生消去、加成、取代等反应 |
D. |
该物质能使溴水或高锰酸钾溶液褪色,能与FeCl3溶液发生显色反应 |
|
下列过程最终无沉淀产生的是 | |
| [ ] | |
A. |
过量氨气通入Al2(SO4)3溶液 |
B. |
CO2通入CaCl2溶液 |
C. |
少量SO2通入BaCl2溶液后再通入过量Cl2 |
D. |
过量CO2通入Na2SiO3溶液 |
|
下列有关实验的叙述中,合理的是 ①用pH试纸测得氯水的pH为2 ②不宜用瓷坩埚灼烧氢氧化钠固体 ③使用容量瓶的第一步操作是先将容量瓶用蒸馏水洗涤后烘干 ④用酸式滴定管量取12.00 mL高锰酸钾溶液 ⑤使用pH试纸测定溶液pH时先润湿,测得溶液的pH都偏小 ⑥实验室配制氯化铁溶液时,可先将氯化铁溶解在盐酸中,再稀释到所需要的浓度 | |
| [ ] | |
A. |
②④⑥ |
B. |
②③⑥ |
C. |
①②④ |
D. |
②③④⑤⑥ |