|
下列关于Na2CO3和NaHCO3的叙述中错误的是 | |
| [ ] | |
A. |
等质量的两种盐分别与足量的盐酸反应,在相同情况下,NaHCO3产生的二氧化碳多 |
B. |
等物质的量的Na2CO3和NaHCO3分别与足量的盐酸反应,在相同情况下产生的二氧化碳体积相等 |
C. |
等物质的量的Na2CO3和NaHCO3分别与同浓度的盐酸反应,Na2CO3消耗盐酸的体积是NaHCO3消耗盐酸体积的2倍 |
D. |
将石灰水加入NaHCO3溶液中不产生白色沉淀,而加入Na2CO3溶液中则产生白色沉淀 |
|
下列反应的离子方程式书写中,正确的是 | |
| [ ] | |
A. |
硫酸与氢氧化钡在溶液中反应:Ba2++SO |
B. |
用Cl2将苦卤中的Br-氧化:Cl2+Br-=Cl-+Br2 |
C. |
用小苏打治疗胃酸过多:HCO |
D. |
用FeCl3溶液腐蚀铜箔制造印刷电路板:Fe3++Cu=Fe2++Cu2+ |
|
设NA为阿伏加德罗常数的值.下列关于0.2 mol·L-1硝酸钡溶液的不正确说法是: | |
| [ ] | |
A. |
1升溶液中所含阴、阳离子总数是0.6 NA |
B. |
1升溶液中含有0.4 NA个NO |
C. |
500毫升溶液中的Ba2+离子浓度是0.2 mol·L-1 |
D. |
500毫升溶液中的NO |
|
下列离子方程式书写正确的是 | |
| [ ] | |
A. |
在FeBr2溶液中通入足量氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
B. |
用石墨电极材料电解NaCl饱和溶液:2Cl-+2H2O |
C. |
向CaCl2溶液中通入二氧化碳气体:Ca2++CO2+H2O=CaCO3+2H+ |
D. |
醋酸与锌粒反应:2H++Zn2+=H2↑+Zn |
|
常温下,将NH4NO3溶于水得到无色溶液,为使溶液中的c(NH | |
| [ ] | |
A. |
加入适量的HNO3,抑制NH |
B. |
加入适量的氨水,使溶液的pH=7 |
C. |
加入适量的水稀释溶液 |
D. |
加入适量的NaOH,使溶液的pH=7 |
|
美国加州Miramal海军航空站安装了一台250 kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600℃~700℃,所用燃料为H2,电解质为熔融的K2CO3.该电池的总反应为:2H2+O2 则下列推断中,正确的是 | |
| [ ] | |
A. |
正极反应为4OH-→2H2O+O2+4e-↑ |
B. |
当电池生成1 mol水时,转移4 mol电子 |
C. |
放电时CO |
D. |
放电时电子向负极移动 |
|
物质的量浓度都为0.1 mol·L-1的CH3COOH与NaOH溶液等体积混合后,下列关系式不正确的是 | |
| [ ] | |
A. |
[Na+]+[H+]=[OH-]+[CH3COO-] |
B. |
[Na+]>[CH3COO-]>[H+]>[OH-] |
C. |
[OH-]=[H+]+[CH3COOH] |
D. |
[CH3COOH]+[CH3COO-]=[Na+] |
|
25℃时,水的电离达到平衡:H2O | |
| [ ] | |
A. |
向水中加入氨水,平衡逆向移动,c(OH-)降低 |
B. |
向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 |
C. |
向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
D. |
将水加热,KW增大,pH不变 |
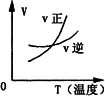
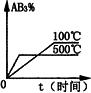
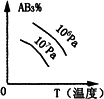
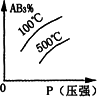
 A2(g)+3B2(g) ΔH>0 (图中AB3%为体系中AB3的体积百分含量,v为反应速率).关于该可逆反应的下列图象不正确的是
A2(g)+3B2(g) ΔH>0 (图中AB3%为体系中AB3的体积百分含量,v为反应速率).关于该可逆反应的下列图象不正确的是