|
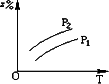
在温度相同,压强分别为p1和p2的条件下,A(g)+2B(g)
| |
| [ ] | |
A. |
p1>p2,n<3 |
B. |
p1<p2,n>3 |
C. |
p1>p2,n>3 |
D. |
p1<p2,n<3 |
|
下列热化学方程式书写正确的是 | |
| [ ] | |
A. |
C(s)+O2(g) |
B. |
2SO2+O2 |
C. |
H2(g)+1/2O2(g) |
D. |
2H2 (g)+O2(g) |
|
哈伯因发明了氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖.现向一密闭容器中充入1 mol N2和3 mol H2,在一定条件下发生反应:N2(g)+3H2(g) | |
| [ ] | |
A. |
温度不变,增大体系的压强 |
B. |
体积、温度不变,增加H2的物质的量 |
C. |
体积、温度不变,增加N2的物质的量 |
D. |
体积不变,降低体系的温度 |
|
某温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g) | |
| [ ] | |
A. |
平衡向逆反应方向移动 |
B. |
C的体积分数减小 |
C. |
平衡不发生移动 |
D. |
A的转化率增大 |
|
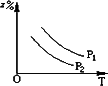
有可逆反应:A(g)+2B(g)
| |
| [ ] | |
A. |
P1>P2,n>3 |
B. |
P1>P2,n<3 |
C. |
P1<P2,n=3 |
D. |
P1<P2,n>3 |
|
在一个固定体积的密闭容器中,加入2 mol A和1 mol B发生反应:2A(g)+B(g) | |
| [ ] | |
A. |
4 mol A+2 mol B |
B. |
2 mol A+1 mol B+3 mol C +1 mol D |
C. |
3 mol C+1 mol D |
D. |
3 mol C+1 mol D+1 mol B |
|
在某容积一定的密闭容器中,可逆反应A(g)+B(g)
| |
| [ ] | |
A. |
P3>P4,y轴表示A的转化率 |
B. |
P3<P4,y轴表示B的体积分数 |
C. |
P3>P4,y轴表示混合气体的密度 |
D. |
P3>P4,y轴表示混合气体的质量 |
|
可逆反应A+B(s) | |
| [ ] | |
A. |
A为气体,C为固体,正反应为放热反应 |
B. |
A为固体,C为气体,正反应为放热反应 |
C. |
A为气体,C为固体,正反应为吸热反应 |
D. |
A、C均为气体,正反应为吸热反应 |
|
对于反应2SO3(g) | |
| [ ] | |
A. |
2体积SO2和足量O2反应,必定生成2体积SO3 |
B. |
其他条件不变,增大压强,化学反应速率必定增大 |
C. |
平衡时,SO2的消耗速率必定等于O2的生成速率 |
D. |
平衡时,SO2浓度必定等于O2浓度的2倍 |