|
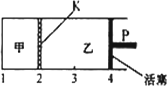
一定温度下的可逆反应:A(s)+2B(g)
| |
| [ ] | |
A. |
保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
B. |
保持活塞位置不变,升高温度,达到新的平衡后,甲中B的体积分数增大,乙中B的体积分数减小. |
C. |
保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
D. |
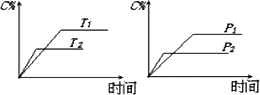
保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图1和图2所示(t1前的反应速率变化已省略)
|
|
可逆反应 :2NO2① 单位时间内生成n mol O2的同时生成2n mol NO2②单位时间内生成n molO2的同时,生成2n mol NO ③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态 ⑥混合气体的平均相对分子质量不再改变的状态 | |
| [ ] | |
A. |
①④⑥ |
B. |
②③⑤ |
C. |
①③④ |
D. |
①②③④⑤⑥ |
|
已建立化学平衡的某可逆反应,当条件改变使化学平衡向正反应方向移动时,下列叙述正确的是 ①生成物的质量分数一定增加 ②生成物产量一定增加 ③反应物的转化率一定增大 ④反应物的浓度一定降低 ⑤正反应速率一定大于逆反应速率 ⑥一定使用催化剂 | |
| [ ] | |
A. |
①②⑤ |
B. |
③④⑤ |
C. |
②⑤ |
D. |
④⑥ |
|
可逆反应aA(s)+bB(g)
| |
| [ ] | |
A. |
达平衡后,加入催化剂则C%增大 |
B. |
达平衡后,若升温,平衡左移 |
C. |
化学方程式中b>c+d |
D. |
达平衡后,增加A的量有利于平衡向右移动 |
|
已知NaHCO3溶液和NaOH溶液反应的离子方程式为:HCO3-+OH- | |
| [ ] | |
A. |
Ba(HCO3)2溶液和硫酸混合:Ba2++SO42-+2H++2HCO3- |
B. |
Ba(HCO3)2溶液和Ba(OH)2溶液混合:Ba2++OH-+HCO3- |
C. |
等体积、等浓度Ca(HCO3)2溶液和NaOH溶液混合: Ca2++2HCO3-+2OH- |
D. |
等体积、等浓度Ba(OH)2溶液和NaHCO3溶液混合:Ba2++OH-+HCO3- |
|
可以证明恒温恒容条件下可逆反应N2+3H2 ①一个N≡N断裂的同时,有3个H-H键断裂 ②一个N≡N键断裂的同时,有6个N-H键断裂 ③混合气体平均相对分子质量不再改变 ④体系压强不再改变 ⑤NH3%、N2%、H2%都不再改变 ⑥密度保持不变 ⑦正反应速率v(H2)=0.6 mol/(L·min),逆反应速率v(NH3)=0.4 mol/(L·min) | |
| [ ] | |
A. |
全部 |
B. |
只有①③④⑤ |
C. |
②③④⑤⑦ |
D. |
只有③⑤⑥⑦ |
|
草酸是二元中强酸,草酸氢钠溶液显酸性.常温下向10 mL 0.01 mol·L-1 NaHC2O4溶液中滴加0.01 mol·L-1 NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是 | |
| [ ] | |
A. |
V (NaOH)=0时,c(H+)=1×10-2 mol·L-1 |
B. |
V (NaOH)<10 mL时,不可能存在c(Na+)=2c(C2O42-)+c(HC2O4-) |
C. |
V (NaOH)=10 mL时,c(H+)=1×10-7 mol/L |
D. |
V (NaOH)>10 mL时,c(Na+)>c(C2O42-)>c(HC2O4-) |
|
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为: 3Zn+2K2FeO4+8H2O 下列叙述不正确的是 | |
| [ ] | |
A. |
放电时负极反应为:Zn-2e-+2OH- |
B. |
充电时阳极反应为:Fe(OH)3-3e-+5OH- |
C. |
放电时每转移3 moL电子,正极有1 mol K2FeO4被氧化 |
D. |
放电时正极附近溶液的碱性增强 |
|
某酸性溶液中只有 Na+、CH3COO-、H+、OH-四种离子.则下列描述正确的是 | |
| [ ] | |
A. |
该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成 |
B. |
该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成 |
C. |
加入适量NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
D. |
加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和 |
|
一定量的Fe和Fe2O3混合物投入250 ml 2 mol/L的HNO3溶液中,反应完全后,无固体剩余,生成1.12 L NO气体(标况),再向反应后溶液中加入1 mol/L的NaOH溶液,要使铁元素全部沉淀下来,所加NaOH溶液的体积最少是 | |
| [ ] | |
A. |
450 ml |
B. |
500 ml |
C. |
400 ml |
D. |
无法确定 |