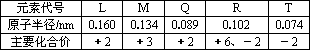|
两种气态烃的混合气体共1 mol,在空气中燃烧得到1.5 mol CO2和2 mol H2O.关于该混合气体的说法正确的是 | |
| [ ] | |
A. |
一定含有甲烷,不含C2H6 |
B. |
一定含C2H6,不含甲烷 |
C. |
一定是甲烷和C2H4的混合气体 |
D. |
一定含甲烷,一定不含C2H4 |
|
下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述 正确的是
| |
| [ ] | |
A. |
L2+与R2-的核外电子数相等 |
B. |
L与T形成的化合物具有两性 |
C. |
氢化物的稳定性为H2T<H2R |
D. |
单质与浓度相等的稀盐酸反应的速率为Q<L |
|
元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构.下列推测不正确的是 | |
| [ ] | |
A. |
同周期元素中X的金属性最强 |
B. |
原子半径X>Y,离子半径X+>Z2- |
C. |
同族元素中Z的氢化物稳定性最高 |
D. |
同周期元素中Y的最高价含氧酸的酸性最强 |
|
已知反应①2FeCl3+2KI ②KClO2+6HCl ③2FeCl2+Cl2=2FeCl3,下列物质的氧化能力强弱顺序正确的是: | |
| [ ] | |
A. |
FeCl3 >Cl2>I2>KClO3 |
B. |
KClO3 >Cl2>FeCl3>I2 |
C. |
Cl2>KClO3>FeCl3>I2 |
D. |
KClO3>Cl2>I2>FeCl3 |
|
为了除去粗盐中的Ca2+、mg2+、SO ①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCI2溶液 正确的操作是 | |
| [ ] | |
A. |
①④②⑤③ |
B. |
④①②⑤③ |
C. |
②⑤④①③ |
D. |
④⑤②①③ |
|
下列离子方程式书写正确的是 | |
| [ ] | |
A. |
将金属Na加入冷水中:2Na+H2O |
B. |
过氧化钠投入水中:Na2O2+H2O |
C. |
在碳酸氢钙溶液中加入少量苛性钠:Ca2-+HCO |
D. |
氢氧化钡溶液与稀硫酸的反应Ba2++OH-+H++SO |
|
用NA表示阿伏加德罗常数的值,下列说法正确的是 | |
| [ ] | |
A. |
1 mol/L 的硫酸100 mL中含有氢离子数目为0.1 NA. |
B. |
标准状况下,22.4 L乙醇所含有的分子总数为NA. |
C. |
7.8 g Na2O2在足量CO2中反应,转移的电子数目为0.2 NA |
D. |
8.0 g Cu2S和CuO的混合物中含有铜原子数为0.1 NA |
|
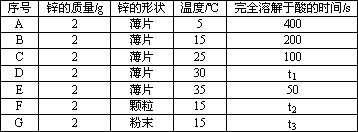
在锌与某浓度的盐酸起反应的实验中,一个学生得到下面的结果:
则下列说法正确的是: ①t1=75 s ②t2>200>t3 ③单位时间内消耗的锌的质量mG>mF>mB | |
| [ ] | |
A. |
① |
B. |
①② |
C. |
只有② |
D. |
全部正确 |
|
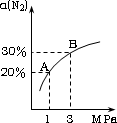
某温度下,对于反应N2(g)+3H2(g)
| |
| [ ] | |
A. |
将1.0 mol氮气、3.0 mol氢气,置于1 L密闭容器中发生反应,放出的热量为92.4 kJ. |
B. |
平衡状态由A变到B时,平衡常数K(A)<K(B). |
C. |
上述反应在达到平衡后,增大压强,H2的转化率提高. |
D. |
升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小. |