|
关于粗盐提纯的下列说法中正确的是 | |
| [ ] | |
A. |
溶解粗盐时,应尽量让溶液稀些,防止食盐不完全溶解 |
B. |
滤去不溶性杂质后,将滤液移至坩埚内加热浓缩 |
C. |
当蒸发到剩余少量液体时,停止加热,利用余热将液体蒸干 |
D. |
将制得晶体转移到新制过滤器中用大量水进行洗涤 |
|
下列各组溶液,只要用试管和胶头滴管,不用任何试剂就可以鉴别的是 | |
| [ ] | |
A. |
KOH和Al2(SO4)3 |
B. |
稀H2SO4和NaHCO3 |
C. |
CaCl2和Na2CO3 |
D. |
Ba(OH)2和NaHSO4 |
|
在氯化铝和氯化镁的混合溶液中,向其中滴加a mL C1 mol·L-1 NaOH之后,改成滴加C2 mol·L-1 HCl,所得沉淀Y(mol)与试剂总体积V(mL)间的关系如下图所示.则所加入NaOH溶液的体积为
| |
| [ ] | |
A. |
9 mL |
B. |
7.5 mL |
C. |
7 ml |
D. |
6 mL |
|
下列液体均处于25℃,有关叙述正确的是 | |
| [ ] | |
A. |
无色溶液中:NH4+、Ag+、PO43-、Cl-能大量共存 |
B. |
水电离产生的c(H+)=10-12 mol·L-1的溶液:K+、Ba2+、Cl-、Br-一定能大量共存 |
C. |
使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl-能大量共存 |
D. |
pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的2倍 |
|
xR2++yH++O2 | |
| [ ] | |
A. |
m=4,R2+ 是氧化剂 |
B. |
2m=y,R3+ 是氧化产物 |
C. |
m=4,R2+ 是还原剂 |
D. |
m=y/2,R3+ 是还原产物 |
|
NA为阿伏加德罗常数,下列叙述正确的是 | |
| [ ] | |
A. |
22.4 L CH4和CH3Cl的混合物所含有的分子数目为NA |
B. |
1 mol过氧化氢分子中共用电子对数为3NA |
C. |
用惰性电极电解1 L浓度均为2 mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2NA个电子转移时,阴极析出6.4 g金属 |
D. |
0.1 mol Na2CO3·10H2O 在晶体中或溶液中,含有的CO32-离子均小于0.1NA |
|
用6.02×1023表示阿伏加德罗常数(NA)的值,下列说法中正确的是 | |
| [ ] | |
A. |
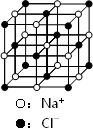
在SiO2晶体中,若含有1 mol Si原子,则含Si-O键数为2NA |
B. |
6.8 g熔融的KHSO4中含有6.02×1022个阳离子 |
C. |
23.4 g NaCl晶体中含有6.02×1022个下图所示的结构单元
|
D. |
用含有0.1 mol FeCl3的饱和溶液制得的氢氧化铁胶体中,胶粒数等于0.1 NA |
|
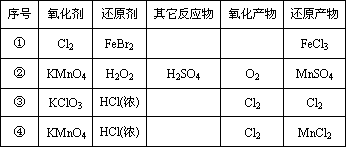
根据下表下列叙述中正确的是:
| |
| [ ] | |
A. |
表中第①组反应的氧化产物一定只有FeCl3(实为Fe3+) |
B. |
氧化性比较:KMnO4>Cl2>Fe3+>Br2>Fe2+ |
C. |
还原性比较:H2O2>Mn2+>Cl- |
D. |
④的离子方程式配平后,H+的化学计量数为16 |
|
把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示,该图为平面透视图),经过一段时间后,首先观察到溶液变红的区域是
| |
| [ ] | |
A. |
Ⅰ和Ⅱ附近 |
B. |
Ⅰ和Ⅳ附近 |
C. |
Ⅱ和Ⅲ附近 |
D. |
Ⅱ和Ⅳ附近 |