|
有3份等质量的小苏打,第1份直接与过量盐酸反应;第2份先加热,使其部分分解后,再与过量盐酸反应;第3份先加热,使其完全分解后,再与过量盐酸反应.假若盐酸的物质的量浓度相同,实际消耗盐酸的体积分别为V1、V2和V3,则V1、V2和V3的大小关系正确的是 | |
| [ ] | |
A. |
V1>V2>V3 |
B. |
V1>V3>V2 |
C. |
V2>V3>V1 |
D. |
V1=V2=V3 |
|
将11.2 g的Mg-Cu混合物完全溶解于足量的硝酸中,收集反应产生的x气体.再向所得溶液中加入适量的NaOH溶液,产生21.4 g沉淀.根据题意推断气体x的成分可能是 | |
| [ ] | |
A. |
0.3 mol NO2 和0.3 mol NO |
B. |
0.1 mol NO 、0.2 mol NO2和0.05 mol N2O4 |
C. |
0.2 mol NO2 和0.1 mol N2O4 |
D. |
0.6 mol NO |
|
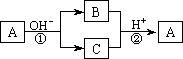
A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X.它们有如下的转化关系(部分产物及反应条件已略去):下列判断正确的是
| |
| [ ] | |
A. |
X元素可能为Al |
B. |
X元素一定为非金属元素 |
C. |
反应①和②互为可逆反应 |
D. |
反应①和②不一定为氧化还原反应 |
|
著名化学家徐光宪获得国家最高科学技术奖,以表彰他在稀土萃取理论方面作出的贡献.已知:金属铈(稀土元素)在空气中易氧化变暗,受热时燃烧,遇水很快反应.(注:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+>I2.)下列说法正确的是 | |
| [ ] | |
A. |
铈溶于氢碘酸的化学方程式可表示为:Ce+4HI |
B. |
用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++2Fe2+ |
C. |
在一定条件下,电解熔融状态的CeO2制Ce,在阴极获得铈 |
D. |
四种的核素13658Ce、13858Ce、14058Ce、14258Ce,它们互称为同素异形体 |
|
有下列四种判断: ①两种弱酸相互反应生成两种强酸; ②两种弱酸盐相互作用后生成两种强酸盐; ③一种弱酸和一种盐溶液作用后,得到一种强酸和一种盐; ④两种酸溶液混合后,溶液的酸性减弱.其中有具体例证的是 | |
| [ ] | |
A. |
①②③④ |
B. |
②③ |
C. |
②③④ |
D. |
①② |
|
下列各组离子在指定溶液中能大量共存的是 ①无色溶液中:K+、Cu2+、Na+、MnO ②pH=11的溶液中:CO ③加入Al能放出H2的溶液中:Cl-、SO ④在由水电离出的c(OH-)=10-13 mol·L-1的溶液中:Na+、Ba2+、Cl-、I- ⑤能使酚酞变红色的溶液:Na+、C1-、S2-、SO ⑥酸性溶液中:Fe2+、Al3+、NO | |
| [ ] | |
A. |
②④⑤ |
B. |
②③④⑤ |
C. |
①②⑤ |
D. |
④⑤⑥ |
|
一定能在下列溶液中大量共存的离子组是 | |
| [ ] | |
A. |
含有大量Al3+的溶液:Na+、 |
B. |
c(H+)=1×10-13 mol·L-1的溶液:Na+、Ca2+、 |
C. |
含有大量Fe3+的溶液:Na+、Mg2+、 |
D. |
含有大量 |
|
甲、乙、丙、丁四个烧杯中,依次分别放入0.1 mol的Na、Na2O、Na2O2、NaOH,然后各加水100 g,待完全溶解后,甲、乙、丙、丁四种溶液的质量分数的关系是 | |
| [ ] | |
A. |
甲<乙<丙<丁 |
B. |
丁<甲<乙<丙 |
C. |
甲=丁<乙=丙 |
D. |
丁<甲<乙=丙 |
|
某燃料电池所用燃料为 H2和空气,电解质为熔融的K2CO3.该电池的总反应为2H2+O2=2H2O,负极反应为H2+CO32-?2e- | |
| [ ] | |
A. |
放电时CO32-向负极移动 |
B. |
该电池正极反应式为:4OH-?4e- |
C. |
电池放电时,电池中CO32-数目逐渐减少 |
D. |
电池放电时,电子经正极、负极、熔融的K2CO3后再回到正极,形成闭合回路 |
|
已知 A、B两种气体在一定条件下可发生反应:2A+B=C+3D+4E.现将相对分子质量为M的A气体m g与适量的B充入一个密闭容器内,恰好完全反应且有少量液滴生成,在相同的温度下测得反应前后压强分别为6.06×106和1.01×107 Pa,且测得反应共放热Q kJ.则该反应的热化学方程式是 | |
| [ ] | |
A. |
2A(g)+B(g)=C(g)+3D(g)+4E(g);ΔH=- |
B. |
2A(g)+B(g)=C(l)+3D(g)+4E(g);ΔH=- |
C. |
2A(g)+B(g)=C(g)+3D(g)+4E(s);ΔH=- |
D. |
2A(g)+B(g)=C(g)+3D(l)+4E(g);ΔH=- |