|
短周期元素X、Y、Z在周期表中的位置如下表所示,下列叙述不正确的是
| |
| [ ] | |
A. |
X是活泼的非金属元素,其最高价氧化物对应的水化物是一种强酸 |
B. |
Y是最活泼的非金属元素,不存在最高价氧化物对应的水化物 |
C. |
Z是较活泼的非金属元素,其最高价氧化物对应的水化物是一种强酸 |
D. |
X、Y、Z的单质中Z的熔点最高 |
| |||||||||||||||||||||||||||||||||||||||||||||
|
草酸(H2C2O4)是二元中强酸,草酸氢钠溶液显酸性.常温下,向10 mL 0.01 mol·L-1 NaHC2O4溶液中滴加0.01 mol·L-1 NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是 | |
| [ ] | |
A. |
V (NaOH)=0时,c(H+)=1×10-2 mol·L-1 |
B. |
V (NaOH)<10 mL时,不可能存在c(Na+)=2c(C2O42-)+c(HC2O4-) |
C. |
V (NaOH)=10 mL时,c(H+)=1×10-7 mol/L |
D. |
V (NaOH)>10 mL时,c(Na+)>c(C2O42-)>c(HC2O4-) |
|
0.1 mol/L的K2S溶液中,有关粒子的浓度大小关系正确的是 | |
| [ ] | |
A. |
c(K+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
B. |
c(K+)+c(S2-)=0.3 mol/L |
C. |
c(K+)=c(S2-)+c(HS-)+c(H2S) |
D. |
c(OH-)=c(H+)+c(HS-)+2c(H2S) |
|
有主族元X、Y、Z,其原子序数依次减小,且均不超过20.X原子的最高能层的电子排布为ns1;Y原子的M能层有2个未成对电子;Z原子的最高能层的p轨道上只有一对成对电子.由这三种元素组成的化合物的化学分子式不可能是 | |
| [ ] | |
A. |
K2SO3 |
B. |
K3PO4 |
C. |
K2SiO3 |
D. |
k2SO4 |
|
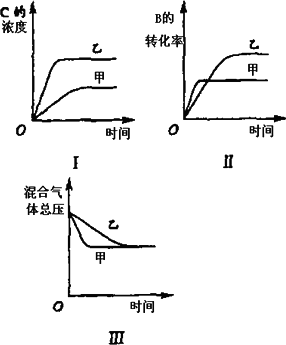
在容积固定的密闭容器中存在如下反应:A(g)+3B(g)
下列判断一定正确的是 | |
| [ ] | |
A. |
图Ⅰ研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高 |
B. |
图Ⅱ研究的是压强对反应的影响,且乙的压强较高 |
C. |
图Ⅱ研究的是温度对反应的影响,且乙的温度较高 |
D. |
图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高 |
|
在常温下10 mL pH=10的KOH溶液中,加入pH=4的一元酸HA溶液至pH刚好等于7(假设反应前后体积不变),则对反应后溶液的叙述正确的是 | |
| [ ] | |
A. |
c(K+)>c(A-) |
B. |
c(H+)=c(OH-)<c(K+)<c(A-) |
C. |
V后≤20 mL |
D. |
V后≥20 mL |
|
某酸式盐NaHY的水溶液显碱性,下列叙述正确的是 | |
| [ ] | |
A. |
H2Y的电离方程式为:H2Y |
B. |
HY-离子的水解方程式为HY-+H2O |
C. |
该酸式盐溶液中离子浓度关系:c(Na+)>c(HY-)>c(OH-)>c(H+) |
D. |
该酸式盐溶液中离子浓度关系:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+) |