|
下列离子方程式与所述事实相符且正确的是 | |
| [ ] | |
A. |
漂白粉溶液在空气中失效:
|
B. |
用浓盐酸与MnO2反应制取少量氯气:
|
C. |
向NaAlO2溶液中通入过量CO2制Al(OH)3:
|
D. |
在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4: 3ClO-+2Fe(OH)3= |
|
按图甲装置进行实验,实验结果如图乙所示.乙中横坐标x表示电路中通过电子的物质的量,纵坐标y表示反应物或生成物的物质的量,下列叙述不正确的是
| |
| [ ] | |
A. |
E表示反应生成铜的物质的量 |
B. |
E表示反应消耗水的物质的量 |
C. |
F表示反应生成氧气的物质的量 |
D. |
F表示反应生成硫酸的物质的量 |
|
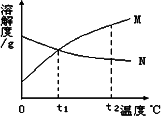
下图是M、N两种物质的溶解度曲线,由溶解度曲线得出以下几条信息,你认为正确的是
| |
| [ ] | |
A. |
t1℃时,M、N两物质溶液溶质质量分数相等 |
B. |
由t1℃升温到t2℃时,N物质溶液溶质质量分数不变 |
C. |
M物质的溶解度大于N物质的溶解度 |
D. |
N物质的溶解度随温度的升高而降低 |
|
某白色粉末可能含有CaCl2、Na2SO4、Ba(NO3)2、K2CO3中的一种或几种.把该粉末放入足量水中,充分搅拌,有白色不溶物产生.过滤,向不溶物中加入稀盐酸,不溶物全部溶解.向滤液中加入BaCl2溶液,没有明显现象.有关该粉末的说法正确的是 | |
| [ ] | |
A. |
肯定有Ba(NO3)2 |
B. |
肯定有K2CO3 |
C. |
肯定有Na2SO4 |
D. |
肯定有CaCl2 |
|
小芳做探究性实验:用称量法测定铁在氧气中燃烧的产物.发现5.6 g铁在充足的氧气中燃烧得到7.82 g固体.小芳排除其他因素可能产生的误差,则实验中得到的固体产物可能是 | |
| [ ] | |
A. |
Fe3O4和Fe的混合物 |
B. |
Fe3O4和FeO的混合物 |
C. |
Fe3O4和Fe2O3的混合物 |
D. |
Fe3O4、FeO和Fe的混合物 |
|
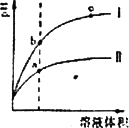
某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如图所示.据图判断正确的是
| |
| [ ] | |
A. |
Ⅱ为盐酸稀释时pH值变化曲线 |
B. |
b点溶液的导电性比c点溶液的导电性强 |
C. |
a点Ka的数值比c点Kc的数值大 |
D. |
b点酸的总浓度大于a点酸的总浓度 |
|
用石墨电解100 mL H2SO4与CuSO4的混合溶液,通电一段时间后,两极均收集到4.48 L气体(标准状况),则原混合溶液中Cu2+的物质的量浓度(mol/L)为 | |
| [ ] | |
A. |
1 |
B. |
2 |
C. |
3 |
D. |
4 |
|
工业上从含硒的废料中提取硒的方法之一是用H2SO4和NaNO3处理废料,获得亚硒酸(H2SeO3)和少量硒酸(H2SeO4),再加入盐酸共热,硒酸被转化为亚硒酸,反应方程式为2 HCl+H2SeO4 | |
| [ ] | |
A. |
H2SeO4氧化性弱于Cl2 |
B. |
H2SeO3氧化性强于H2SO3 |
C. |
H2SeO3氧化性弱于SO2 |
D. |
析出1 molSe需H2SeO3、SO2、H2O各1 mol |