|
X、Y和Z是第三周期的三种元素.已知:X的单质与水在常温条件下就能剧烈反应,Y的最高价氧化物对应的水化物是一种酸性最强的酸;Z能形成氯化物ZCl5.上述三种元素原子的半径由大到小的顺序是 | |
| [ ] | |
A. |
X,Z,Y |
B. |
Y,Z,X |
C. |
Z,Y,X |
D. |
X,Y,Z |
|
根据元素周期表和元素周期律,下列推断正确的是 | |
| [ ] | |
A. |
HF、HCl、HBr、HI的酸性逐渐增强,说明F、Cl、Br、I的非金属性逐渐增强 |
B. |
元素R最高正价为+7价,表明R元素属于ⅦA族元素 |
C. |
若M+和R2-具有相同的电子层结构,则原子半径:M<R |
D. |
从元素在周期表中的位置可以推断,硅和锗都可用作半导体材料 |
|
下列关于物质的用途或变化,说法正确的是 | |
| [ ] | |
A. |
Al2O3熔点很高,可用作耐火材料 |
B. |
高纯度的硅单质用于制作光导纤维 |
C. |
铝热反应是炼铁最常用的方法 |
D. |
N2与O2在放电条件下直接化合生成NO2 |
|
下列关于SiO2和CO2的叙述不正确的是 | |
| [ ] | |
A. |
都是共价化合物 |
B. |
都是酸性氧化物,都能与强碱溶液反应 |
C. |
都能溶于水且与水反应生成相应的酸 |
D. |
SiO2可用于制光导纤维,干冰可用于人工降雨 |
|
2011年3月11日,日本大地震引起全世界关注,中国核事故应急协调委员会4月1日发布,内地除西藏外都检测到 | |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
单质铯的金属性比单质钠弱 |
|
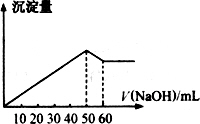
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量之比为
| |
| [ ] | |
A. |
6∶1 |
B. |
3∶1 |
C. |
2∶1 |
D. |
1∶2 |
|
a、b、c三种元素的原子序数均小于20,a、b两元素的阳离子和c元素的阴离子都有相同的电子层结构,a原子的半径大于b原子的半径,则三种元素的原子序数的关系是 | |
| [ ] | |
A. |
b>a>c |
B. |
a>b>c |
C. |
c>b>a |
D. |
a>c>b |